
����Ŀ��̼Ԫ�صĵ����ж�����ʽ����ͼ������C60��ʯī�ͽ��ʯ�Ľṹͼ�� 
�ش��������⣺
��1�����ʯ��ʯī��C60��̼���ܶ���̼Ԫ�صĵ�����ʽ�����ǻ�Ϊ ��
��2�����ʯ��ʯīϩ��ָ����ʯī����̼ԭ�ӵ��ӻ���ʽ�ֱ�Ϊ�� ��
��3��C60�������壬ʯī�������壮
��4��ʯī�����У�����C��C���ļ���Ϊ142pm�������ʯ��C��C���ļ���Ϊ154pm����ԭ���ǽ��ʯ��ֻ����C��C������ۼ�����ʯī���ڵ�C��C�䲻���������ۼ�����������
��5�����ʯ����������̼ԭ�ӣ���̼ԭ�Ӱ뾶Ϊr�����ʯ�����ı߳�Ϊa������Ӳ��Ӵ�ģ�ͣ���r=a����ʽ��ʾ̼ԭ���ھ����еĿռ�ռ��������Ҫ�����������
���𰸡�
��1��ͬ��������
��2��sp3��sp2
��3�����ӣ����
��4���ң��ң���
��5��8��![]() ��
��![]()
���������⣺��1�����Ǻ���̼Ԫ�صIJ�ͬ���ʣ���Ϊͬ�������壬���Դ��ǣ�ͬ�������壻��2�����ʯ��̼ԭ���γ��������ۼ���Ϊsp3�ӻ���ʯīϩΪƬ��ṹ���ӻ�����Ϊsp2�ӻ������Դ��ǣ�sp3��sp2����3��C60���������Ϊ60��̼ԭ����ɵ�C60���ӣ����ڷ��Ӿ��壻ʯīƬ�����Թ��ۼ���ϣ�Ƭ��֮���Է��Ӽ���������ϣ�Ϊ��Ͼ��壬���Դ��ǣ����ӣ���ϣ���4�����ʯ��̼ԭ����sp3�ӻ����γ������ӻ������ȫ���γɦҼ���ʯī��̼ԭ����sp2�ӻ����γ������ӻ����������һ��Ϊ�ӻ���p����������ӻ�����γɦҼ�����δ�ӻ�p����γɦм������Դ��ǣ��ң��ң��У���5�������ж�������Ϊ�� ![]() =1����������Ϊ��
=1����������Ϊ�� ![]() =3����������Ϊ4��������8��̼ԭ�ӣ������ں����ĸ�̼ԭ�ӣ�����Խ��߳������ĸ�̼ԭ��ֱ����ͬ����
=3����������Ϊ4��������8��̼ԭ�ӣ������ں����ĸ�̼ԭ�ӣ�����Խ��߳������ĸ�̼ԭ��ֱ����ͬ���� ![]() =8r��r=
=8r��r= ![]() a��̼ԭ�ӵ����Ϊ��
a��̼ԭ�ӵ����Ϊ�� ![]() ���������Ϊ��a3 �� ̼ԭ�ӵĿռ�������Ϊ��
���������Ϊ��a3 �� ̼ԭ�ӵĿռ�������Ϊ�� ![]() =
= ![]() =
= ![]() �����Դ��ǣ�8��
�����Դ��ǣ�8�� ![]() ��
�� ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ�������Ŀ��
��1������֮��Ϊ7��6����������CO��NO��������֮��Ϊ����ԭ����֮��Ϊ����ͬ�����µ����֮��Ϊ ��
��2������mgij���壬����˫ԭ�ӷ��ӹ��ɣ�����Ħ������ΪMgmol��1 �� �������ӵ�������NA��ʾ���ٸ���������ʵ���Ϊmol��
�ڸ���������ԭ������Ϊ����
�۸������ڱ�״���µ����ΪL��
�ܸ���������1Lˮ�У������Ƿ�Ӧ��������Һ�����ʵ���������Ϊ ��
�ݸ���������ˮ���γ�VL��Һ������Һ�����ʵ���Ũ��ΪmolL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������OH�������·���ˮ�ⷴӦ�� O2NC6H4COOC2H5+OH��O2NC6H4COO��+C2H5OH
���ַ�Ӧ��ij�ʼŨ�Ⱦ�Ϊ0.050molL��1 �� 15��ʱ���O2NC6H4COOC2H5��ת���ʦ���ʱ��仯�����������ʾ���ش��������⣺
t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
��/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
��1����ʾ����÷�Ӧ��120��180s��180��240s�����ƽ����Ӧ���������Ƚ����ߴ�С�ɵó��Ľ����� ��
��2����ʽ����15��ʱ�÷�Ӧ��ƽ�ⳣ�� ��
��3��Ϊ���O2NC6H4COOC2H5��ƽ��ת���ʣ������ʵ����Ʒ�Ӧ�¶��⣬���ɲ�ȡ�Ĵ�ʩ����Ҫ��д����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����Թܷ���ʢ��25��ʱ����ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ���ٵ���5mL���ᣬ�Իش��������⣮ 
��1��ʵ���й۲쵽�������� ��
��2���������������ԭ���� ��
��3���ɴ���֪��MgCl2��Һ��H2��������������ڡ�����С�ڡ����ڡ���þƬ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������У������ˣ������������ܽ⣻��ȡҺ���Լ�����ȡ�����Լ���һ��Ҫ�õ�����������
A���٢ڢ� B���ܢ�
C���٢� D���٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п��һ��Ӧ�ù㷺�Ľ�����Ŀǰ��ҵ����Ҫ���á�ʪ��������ұ��п��ij��п�����Ҫ�ɷ���ZnS������������FeS�������ɷ֣�������Ϊԭ����п�Ĺ���������ͼ��ʾ�� 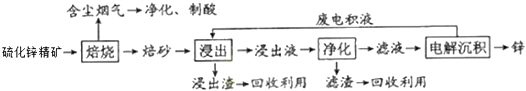
�ش��������⣺
��1����п����ı������������յķ���¯�н��У���������ɰ����Ҫ�ɷֵĻ�ѧʽΪ ��
��2�����չ����в����ĺ��������ɾ������ᣬ��������ں�����������
��3������Һ�������������м������Ҫ����Ϊ �� �������� ��
��4�������������е������������壬��������Pb��Ag�Ͻ���Ե缫�������ݳ��������� ��
��5���Ľ���пұ�����գ������ˡ���ѹ�������ȫʪ�����̣���ʡ�������¿�����Ⱦ�ı��չ��̣��ֿɻ��һ���ɹ�ҵ��ֵ�ķǽ������ʣ�����ѹ������з�����Ҫ��Ӧ�����ӷ���ʽΪ ��
��6���ҹ��Ŵ������á�������ұ��п��������Ӧ�������칤������йء�������Ǧ���ļ��أ���¯��ʯʮ�װ����һ����ڣ�����Ȼ�������ú̿����ʢ�������н������ͺ죬����������ٹ�ȡ����������ǦҲ��������п������Ҫ��Ӧ�Ļ�ѧ����ʽΪ �� ��ע��¯��ʯ����Ҫ�ɷ�Ϊ̼��п����Ǧ��ָ����п����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.�ö��Ե缫���Na2SO4��Һ������������������ʵ���֮��Ϊ1��2
B.��ԭ��صĸ����͵��ص������϶��Ƿ���ʧ���ӵ�������Ӧ
C.�ö��Ե缫��ⱥ��NaCl��Һ������1 mol����ת�ƣ�������1 molNaOH
D.�Ʋ������������ȶ�п�������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ�ǿ�ѧ�����Ʊ���һ����Ҫ����������ɵ�ֱֻ�ӻ��϶��ɣ�����ˮ���õIJ���֮һΪNH3 �� ��ش��������⣺
��1��Na3N�������γɵ������д�����ĵ���ʽ�� ��
��2��Na3N��ˮ��Ӧ�������������Ӧ���ͣ���д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3��Na+��N3���İ뾶��ϵ��Na+�����������������=����N3�� ��
��4��Mg3N2������ķ�Ӧ�������Σ��õ���ʽ��ʾ����ֻ�������Ӽ����ε��γɹ��� �� д����һ���εĵ���ʽ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯�ƣ�CaH2�������ǵ�ɽ�˶�Ա���õ���Դ�ṩ�����⻯��Ҫ�ܷⱣ�棬һ���Ӵ���ˮ�ͷ�����Ӧ�����������ƺ��������⻯����һ����������������Ӧ���ɵIJ��ﲻֻһ�֣��⻯��ͨ��������������Ƽ�����ȡ����ͼ1��ģ����ȡװ�ã� 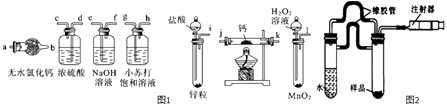
��ش��������⣺
��1����������װ����ȡ�⻯��ʱ��������������˳��Ϊ���������ӿڵ���ĸ��ţ���
i��������������a
��2��װ����ˮ�Ȼ���װ�õ������� ��
��3������������ʵ��װ�ý���ʵ�飬ʵ�鲽�����£����װ�������Ժ�װ��ҩƷ����Һ©�����������밴��ȷ��˳���������в���ı�ţ���
A.���ȷ�Ӧһ��ʱ��
B.�ռ����岢�����䴿��
C.�رշ�Һ©������
D.ֹͣ���ȣ������ȴ
��4����ͬѧ�����һ��ʵ�飬�ⶨ����ʵ���еõ����⻯�ƵĴ��ȣ�����������ʵ�鲽�裺
����Ʒ������
�ڼ�����Һ���ѧʽ�������裻
������������ƣ���ϴ�ӣ�����
�ܳ���̼��ƣ�
��5������������Ŀ�и�����װ�ã��Լ�����ѡ�����ʵ�飬�û�ѧ����֤�������к����⻯�ƣ�д��ʵ���Ҫ���輰�۲쵽������ ��
��6����ͬѧ����ͼ2��ʾװ�òⶨ����ʵ���еõ����⻯�ƵĴ��ȣ�����ȡ46mg���Ƶõ��⻯����Ʒ����¼��ʼʱע������˨ͣ����lO.00mL�̶ȴ�����Ӧ����������ȴ����˨����ͣ����57.04mL�̶ȴ�����������������ڱ�״���²ⶨ������ͨ����������Ʒ���⻯�ƵĴ��ȣ� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com