
����Ŀ��������Ԫ��a��b��c��d��ԭ��������������b��cΪ���ֳ����Ľ���Ԫ�أ�a��b��c��d������������Ӧ��ˮ��������Ϊ�ס��ҡ�������������֮�������ͼ��ʾ�ķ�Ӧ��ϵ(ͼ���á�--���������������ʼ��ܷ�����Ӧ)�������ж�һ����ȷ����
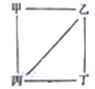
A. �����Ӱ뾶:d>b>c>a
B. �����ʵ�����ba3��b3a�����������������
C. d������ϼۺ���ͻ��ϼ۵Ĵ�����Ϊ6
D. b��d��ɵĻ������ˮ��Һ������
���𰸡�B
��������������Ԫ��a��b��c��d��ԭ��������������b��cΪ���ֳ����Ľ���Ԫ�أ�a��b��c��d������������Ӧ��ˮ��������Ϊ�ס��ҡ������������ݹ�ϵͼ��������ܹ���Ӧ����˵��cΪAlԪ�أ���Ϊ������������bΪ�ƣ���Ϊ�������ƣ����ܹ���Ͷ���Ӧ��˵���Ͷ�Ϊ�ᣬ��aΪN����Ϊ���ᣬdΪS��Cl����Ϊ���������ᡣA. ���Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�����Ӱ뾶Խ�������Ӱ뾶a>b>c����A����B. �����ʵ�����NaN3��Na3N������������֮��Ϊ2:4=1:2����B��ȷ��C. dΪS��Cl������ϼۺ���ͻ��ϼ۵Ĵ�����Ϊ4��6����C����D. b��d��ɵĻ�����Ϊ���ƻ��Ȼ��ƣ���������ˮ�⣬��Һ�Լ��ԣ���D����ѡB��


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ��״���£�CO��һ����ɫ����ζ���ж������壬������ˮ�����ᡢ�����Һ������Ӧ����֪�Ҷ��ᾧ����ȷֽ�ķ���ʽΪ��H2C2O4��2H2O![]() 3H2O+CO2��+CO�����������������ظ��ţ������������װ����֤��Ӧ�����к���CO2��CO��װ�ò����ظ�ʹ�ã����ƾ���ƿ���������Դ����ش��������⣺
3H2O+CO2��+CO�����������������ظ��ţ������������װ����֤��Ӧ�����к���CO2��CO��װ�ò����ظ�ʹ�ã����ƾ���ƿ���������Դ����ش��������⣺
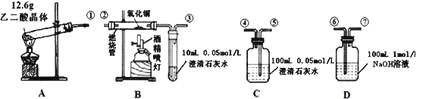
��1������װ��A�����Եķ�����
��2���������������Ӹ������������ֱ�ʾ�ӿڵ�����˳��
�١�
��3��֤��CO���ڵ�ʵ��������
��4����ʵ��β�������ķ�����
��5��������������ݣ��������Ӧ����ַ����Ҳ���������ȫ���ų�����������Һ��ַ�Ӧ����ʾ��B��C�г���ʯ��ˮ���ȱ���ǣ����ֱ���壩��D�����ʼ���Ӧ�����ʵ����ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D����ѧ��ѧ�����Ļ���������ᴿ�Ļ���װ�á�
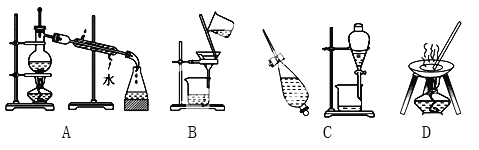
����ݻ���������ᴿ��ԭ�����ش�������ʵ������Ҫʹ����һ��װ�ã���A��B��C��D�����ʵ��Ŀո��С�
��1���ӵ�ˮ����ȡ��_____________________________��
��2��ʵ������ȡ����ˮ_____________________________��
��3��ȥ�����е���ɳ_____________________________��
��4���뺣ˮɹ��ԭ���������___________________________��
���������а������ʣ���HCl�����Cu ��CO ��CO2 �ݽ��ʯ ��KMnO4���� ��Ba(OH)2��Һ ������KAl(SO4)2
��1�����ڵ��ʵ���_________�������������������_________������״̬�ܵ���ĵ������_________��(���������ʵ����)
��2��д��Ba(OH)2��ˮ�еĵ��뷽��ʽ��____________________________________________��
��3����˫���ű�ʾ�÷�Ӧ�е���ת�Ƶķ������Ŀ_______
2KMnO4+16HCl=5Cl2��+2MnCl2+2KCl+8H2O
����0.8mol��ԭ������������ת�Ƶ��ӵ����ʵ�����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CaC2����ľ����ṹ��NaCl��������ƣ���ͼ��ʾ������CaC2�����к��е���������C ![]() �Ĵ��ڣ�ʹ������һ���������������й���CaC2�����˵������ȷ���ǣ� ��
�Ĵ��ڣ�ʹ������һ���������������й���CaC2�����˵������ȷ���ǣ� �� 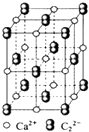
A.1��Ca2+��Χ��������ҵȾ����C22����ĿΪ6
B.�þ����е���������F2�ǵȵ�����
C.6.4��CaC2�����������0.1mol
D.��ÿ��Ca2+��������������Ca2+����12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������֧�Թ��У���������ֽ���������Ļ�ѧ��Ӧ���������ǣ�������
�Թ� | �¶� | ��������Ũ�� | ���� |
A | ���£�25�棩 | 12% | �� |
B | ˮԡ���ȣ�50�棩 | 4% | �� |
C | ˮԡ���ȣ�50�棩 | 12% | �� |
D | ���£� 25�棩 | 4% | �� |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.�⻯��(NaH) ��һ�����ӻ������ˮ��ų�����������һ�ּ��ҪӦ�����л��ϳɺʹ�����Ϸ��档������Ϣ������и���:
��1���⻯�Ƶĵ���ʽΪ_____________________________��
��2���⻯����ˮ��Ӧ�Ļ�ѧ����ʽΪ_____________________����Ӧ��������Ϊ___________���÷�Ӧ�����У����ƻ��Ļ�ѧ����_____________(����ţ���ͬ)���γɵĻ�ѧ����______________��
�����Ӽ� �ڼ��Թ��ۼ� �۷Ǽ��Թ��ۼ�
II.���ж�����Ԫ��X �γɵĵ���A��NaOH��Һ��Ӧ��������ת����ϵ: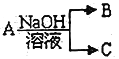 ��(����������ˮ������ʡ��δ��ʾ����)��
��(����������ˮ������ʡ��δ��ʾ����)��
��1�����³�ѹ�£���A Ϊ�ǽ�����̬���ʣ������ڵ��ӹ�ҵ��������Ҫ����;����ҵ��ȡA��ѧ����ʽΪ________________________________________________��
��2����A Ϊ�������ʣ�C Ϊ���壬��A ��NaOH ��Һ��Ӧ�����ӷ���ʽΪ_____________________________��A ����������ˮ������NaOH ��Һ��Ӧ�����ӷ���ʽΪ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʻ�Ϸ�����ѧ��Ӧ���ҷ�Ӧ�������ӷ�Ӧ���ǣ�( )
A. H2��O2��Ӧ����ˮ
B. пƬͶ��ϡ������
C. KClO3(����)��MnO2(����)��ϼ�����O2
D. NaOH��Һ��K2SO4��Һ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������CuMn2O4�����ڳ����´����������е�һ����̼�ͼ�ȩ��HCHO����
��1����Ԫ��λ�ڵ������ڵڢ�B�壮��̬Mn2+�ĺ�������Ų�ʽΪ �� NO3���Ŀռ乹��Ϊ ��
��2��HCHO�к��еĦҼ��ͦм���Ŀ֮��Ϊ ��
��3����ɽ������ҽ��к��ж��������ȴʱZnS��HgS��������ԭ����
��4��Cu3N�γɵľ���ṹ��ͼ��ʾ������ͬһ��N3��������Cu+������Cu+�İ뾶Ϊa pm��N3���İ뾶Ϊb pm����Cu3N���ܶ�Ϊgcm��3 �� ��ֻ��ʽ�����ü����������������ӵ�������NA��ʾ��1pm=10��10 cm�� 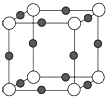
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��������VB2����������ع���ʱ������ӦΪ��11O2+4VB2�T2V2O5+4B2O3 �� �Ըõ����Ϊ��Դ��ʹ�ö��Ե缫�������ͭ��Һ��ʵ��װ����ͼ��ʾ�������·��ͨ��0.04mol����ʱ��Bװ���ڹ��ռ���0.448L���壨��״������������˵����ȷ���ǣ� �� 
A.VB2�缫�����ĵ缫��ӦΪ��2VB2+11H2O��22e���TV2O5+2B2O3+22H+
B.��Bװ���ڵ�Һ�����Ϊ400mL����CuSO4��Һ�����ʵ���Ũ��Ϊ0.025mol/L
C.�������У�b�缫�������к�ɫ����������Ȼ�������ݲ���
D.���·�е�����a�缫����b�缫
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com