
【题目】纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用.
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为、 . 某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图1: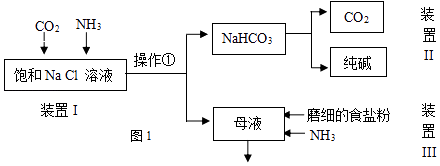
已知:几种盐的溶解度
NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
(2)①写出装置I中反应的化学方程式 . ②从平衡移动角度解释该反应发生的原因 .
③操作①的名称是 .
(3)写出装置II中发生反应的化学方程式 .
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用.
(5)该流程中可循环利用的物质是
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是 . a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4 , 干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量.
【答案】
(1)Ca(OH)2;Na2CO3
(2)NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl;在溶液中存在下述两种平衡NH3+H2O?NH3?H2O?NH4++OH﹣,CO2+H2O?H2CO3?H++HCO3﹣,OH﹣与H+结合生成水,促进两平衡正向移动,使溶液中的NH4+和HCO3﹣浓度均增大,由于NaHCO3溶解度小,因此HCO3﹣与Na+结合生成NaHCO3,固体析出使得反应发生;过滤
(3)2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(4)在母液中含有大量的NH4+和Cl﹣,存在平衡NH4Cl(s)?NH4++Cl﹣,通入氨气增大NH4+的浓度,加入磨细的食盐粉,增大Cl﹣的浓度,使上述平衡逆向移动,促使氯化铵结晶析出
(5)氯化钠和二氧化碳
(6)c
【解析】解:(1)工业上除去Mg2+用含有OH﹣的可溶性碱、除去Ca2+用含有CO32﹣的可溶性盐,且这两种试剂必须价格低廉,除去镁离子用氢氧化钙、除去钙离子用碳酸钠,所以答案是:Ca(OH)2;Na2CO3;(2)①NaCl、CO2、NH3、H2O发生反应生成NaHCO3和NH4Cl,反应方程式为NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl,所以答案是:NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl;
②在溶液中存在下述两种平衡NH3+H2ONH3H2ONH4++OH﹣,CO2+H2OH2CO3H++HCO3﹣,OH﹣与H+结合生成水,促进两平衡正向移动,使溶液中的NH4+和HCO3﹣浓度均增大,由于NaHCO3溶解度小,因此HCO3﹣与Na+结合生成NaHCO3,固体析出使得反应发生,所以答案是:在溶液中存在下述两种平衡NH3+H2ONH3H2ONH4++OH﹣,CO2+H2OH2CO3H++HCO3﹣,OH﹣与H+结合生成水,促进两平衡正向移动,使溶液中的NH4+和HCO3﹣浓度均增大,由于NaHCO3溶解度小,因此HCO3﹣与Na+结合生成NaHCO3,固体析出使得反应发生;③分离沉淀和溶液采用过滤方法,所以该操作名称是过滤,所以答案是:过滤;(3)受热条件下,碳酸氢钠分解生成碳酸钠、二氧化碳和水,反应方程式为2NaHCO3 ![]() Na2CO3+H2O+CO2↑,所以答案是:2NaHCO3
Na2CO3+H2O+CO2↑,所以答案是:2NaHCO3 ![]() Na2CO3+H2O+CO2↑;(4)在母液中含有大量的NH4+和Cl﹣,氯化铵存在溶解平衡,增大离子浓度抑制其溶解,所以在母液中含有大量的NH4+和Cl﹣,存在平衡NH4Cl(s)NH4++Cl﹣,通入氨气增大NH4+的浓度,加入磨细的食盐粉,增大Cl﹣的浓度,使上述平衡逆向移动,促使氯化铵结晶析出,所以答案是:在母液中含有大量的NH4+和Cl﹣,存在平衡NH4Cl(s)NH4++Cl﹣,通入氨气增大NH4+的浓度,加入磨细的食盐粉,增大Cl﹣的浓度,使上述平衡逆向移动,促使氯化铵结晶析出;(5)装置III中从母液中能分离出氯化钠,装置II中得到二氧化碳,装置I中需要二氧化碳和氯化钠,所以能循环利用的是氯化钠和二氧化碳,所以答案是:氯化钠和二氧化碳;(6)a.只有氯化钙能和碳酸钠反应生成碳酸钙,根据碳酸钙的量计算碳酸钠的量,所以该方案可以,故a不选;b.只有碳酸钠能和稀硫酸反应生成二氧化碳,根据二氧化碳的量计算碳酸钠的量,所以该方案可以,故b不选;c.碳酸根离子和氯离子都能和银离子反应生成白色沉淀,无法计算碳酸钠的量,所以该方案不可以,故c选;故选c.
Na2CO3+H2O+CO2↑;(4)在母液中含有大量的NH4+和Cl﹣,氯化铵存在溶解平衡,增大离子浓度抑制其溶解,所以在母液中含有大量的NH4+和Cl﹣,存在平衡NH4Cl(s)NH4++Cl﹣,通入氨气增大NH4+的浓度,加入磨细的食盐粉,增大Cl﹣的浓度,使上述平衡逆向移动,促使氯化铵结晶析出,所以答案是:在母液中含有大量的NH4+和Cl﹣,存在平衡NH4Cl(s)NH4++Cl﹣,通入氨气增大NH4+的浓度,加入磨细的食盐粉,增大Cl﹣的浓度,使上述平衡逆向移动,促使氯化铵结晶析出;(5)装置III中从母液中能分离出氯化钠,装置II中得到二氧化碳,装置I中需要二氧化碳和氯化钠,所以能循环利用的是氯化钠和二氧化碳,所以答案是:氯化钠和二氧化碳;(6)a.只有氯化钙能和碳酸钠反应生成碳酸钙,根据碳酸钙的量计算碳酸钠的量,所以该方案可以,故a不选;b.只有碳酸钠能和稀硫酸反应生成二氧化碳,根据二氧化碳的量计算碳酸钠的量,所以该方案可以,故b不选;c.碳酸根离子和氯离子都能和银离子反应生成白色沉淀,无法计算碳酸钠的量,所以该方案不可以,故c选;故选c.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
(1)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,则该溶液呈性,原因是;(用离子方程式表示)
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于;
(3)已知在H2S溶液中存在下列平衡:H2S═HS﹣+H+①向H2S溶液中加入NaOH固体时,(不考虑温度变化)电离平衡向移动,(填“左”或“右”)c(H+) . (填“增大”、“减小”或“不变”)
②向H2S溶液中加入NaHS固体时,电离平衡向移动,(填“左”或“右”)c(S2﹣) . (填“增大”、“减小”或“不变”)
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是(填“A”或“B”);设盐酸中加入的Zn质量为m1 , 醋酸溶液中加入的Zn质量为m2 . 则m1m2 . (选填“<”、“=”、“>”) 
(5)难溶电解质在水溶液中存在溶解平衡.某MgSO4溶液里c(Mg2+)=0.002molL﹣1 , 如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于;(该温度下Mg(OH)2的Ksp=2×10﹣11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,用0.1000mol/L NaOH溶液滴定25.00mL 0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如图所示.下列说法不正确的是( ) 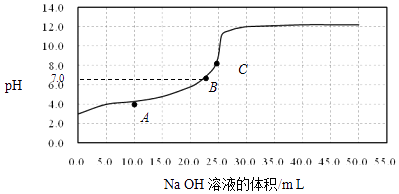
A.在A点:c(HX)>c(Na+)>c(X﹣)
B.在B点,溶液中c(H+)=c(OH﹣)
C.C点溶液中存在的主要平衡是X﹣+H2OHX+OH﹣
D.0.05mol/L NaX溶液的pH≈9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然产物萜类化合物eudesmane合成路线片段如图.(某些反应条件省略) 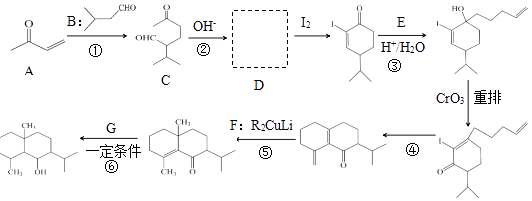
已知:
i.RCHO+R′﹣CH2﹣CHO ![]()
![]() +H2O
+H2O
ii.RMgX+ ![]() →
→ 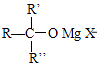
![]()

iii. 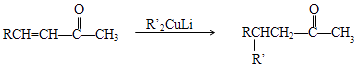
回答下列问题:
(1)A中的官能团名称是羰基、 .
(2)反应②的化学方程式是 ![]() .
.
(3)反应③中试剂E的结构简式是 .
(4)反应④的另一种产物是 .
(5)F的结构简式是 .
(6)G的电子式是 .
(7)D有多种同分异构体,满足下列条件的有种,写出其中任意一种. a.能发生银镜反应b.结构为六元环状c.环上有3种氢原子
(8)以CH3CH2OH与CH3COCH3为原料,结合已知信息选用必要的无机物合成B,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上标明试剂和反应条件).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如图所示.下列有关说法正确的是( ) 
A.锌片发生氧化反应作阴极
B.电子从铁片经过导线流向锌片
C.铁片上电极反应为:O2+2H2O+4e→4OH﹣
D.该装置可用于研究外加电流阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃A在一定条件下可以按下面的框图进行反应. 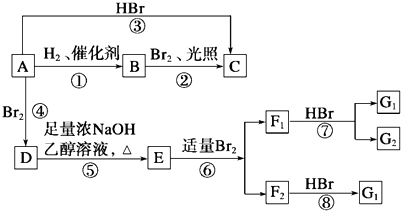
已知:D是 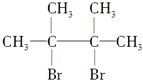 .
.
请填空:
(1)A的结构简式是 , 其名称为 .
(2)框图中属于取代反应的是(填数字代号).
(3)框图中①、③、⑥属于反应.
(4)G1的结构简式是
(5)写出由D→E的化学方程式:;写出由E→F2的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Z由如下反应得到:C4H9Br ![]() Y
Y ![]() Z,Z的结构简式不可能是( )
Z,Z的结构简式不可能是( )
A.CH3CH2CHBrCH2Br
B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3
D.CH2BrCBr(CH3)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com