
| A、pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 |
| B、pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C、pH=6的醋酸用水稀释100倍,PH=8 |
| D、在25 mL 0.1 mol?L-1NaOH溶液中,滴入0.1 mol?L-1的CH3COOH溶液至混合溶液pH=7时,则滴加CH3COOH溶液的体积大于25 mL |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
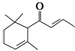 分子式为C13H20O,有关该化合物的下列说法正确的是( )
分子式为C13H20O,有关该化合物的下列说法正确的是( )| A、一定条件下1mol该化合物最多可与2mol氢气加成 |
| B、该化合物可发生银镜反应 |
| C、1mol该化合物完全燃烧消耗19mol O2 |
| D、该化合物可发生加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、互称为同分异构体的物质不可能具有相同的通式 |
| B、通式相同的不同有机物一定属于同系物 |
| C、互为同分异构体的物质之间物理性质一定不同,但化学性质一定相似 |
| D、具有相同官能团的有机物不一定是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl |
| B、H2SO4 |
| C、H2C2O4(草酸) |
| D、H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和冷水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| B、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| C、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| D、FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘在酒精中的溶解度很大,所以可以用酒精萃取碘水 |
| B、滤纸不能用来过滤强酸、强碱是因为强酸、强碱有腐蚀性 |
| C、往溶液中滴加氯化钡,有白色沉淀生成,说明溶液中有硫酸根离子 |
| D、蒸发中当出现大量固体时,停止加热,利用余热把剩余溶液蒸干 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH=CH3COO-+H+ |
| B、Br-+H2O?HBr+OH- |
| C、CO32-+2H2O?H2CO3+2OH- |
| D、NH4++2H2O?NH3?H2O+H3O+ |
| E、NH4++2H2O?NH3?H2O+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、集气瓶中气体的黄绿色变浅 |
| B、集气瓶中有火星出现 |
| C、集气瓶内壁上有油状液滴出现 |
| D、集气瓶口有白雾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com