
【题目】在第ⅦA族元素的氢化物中,最容易分解成单质的是
A.HIB.HBrC.HClD.HF
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH- ΔH>0。下列叙述正确的是( )
H++OH- ΔH>0。下列叙述正确的是( )
A. 将水加热,Kw增大,pH不变
B. 向水中加入少量NaOH溶液,平衡逆向移动,c(OH-)减小
C. 向水中加入少量冰醋酸,平衡正向移动,c(H+)增大
D. 向水中加入少量固体NaHSO4,c(H+)增大,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下不能实现的是( )
A. 饱和NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
B. MgCl2(aq)![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO
C. Al2O3![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3
Al(OH)3
D. Fe2O3![]() FeCl3(aq)
FeCl3(aq)![]() 无水FeCl3
无水FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.02 mol·L-1的Ba(OH)2溶液100mL和0.02 mol·L-1NaHSO4溶液100mL混合,若忽略溶液体积变化,则混合后的溶液( )
A.pH=12B.溶质的物质的量浓度=0.02 mol·L-1
C.pH=2D.由水电离的产生的c(H+)=1.0×10-2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是
A.分子间作用力;分子间作用力;非极性键
B.分子间作用力;分子间作用力;极性键
C.分子间作用力;极性键;分子间作用力
D.分子间作用力;分子间作用力;非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。

则下列热化学方程式不正确的是( )
A. 1/2A2(g)+1/2B2(g)=AB(g) ΔH=-91.5kJ·mol-1
B. A2(g)+B2(g)=2AB(g) ΔH=-183kJ·mol-1
C. 2AB(g)=A2(g)+B2(g) ΔH=+183kJ·mol-1
D. 1/2A2(g)+1/2B2=AB(g) ΔH=+91.5kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇可以发生下列化学反应。在反应里乙醇分子断裂C-O键而失去羟基的是( )
A. 乙醇与乙酸的酯化反应 B. 乙醇与金属钠反应
C. 乙醇在浓H2SO4存在下发生消去反应 D. 乙醇的催化氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下:
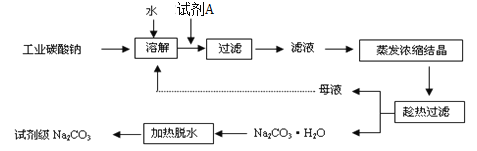
碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
![]()
请回答下列问题:
①试剂A是_______,“母液”中除了含有Na+、CO32-、OH-外,还含有_____等离子,过滤要“趁热”的目的是______。
②检验试剂Na2CO3中Cl-和SO42-是否除尽,选用的试剂及加入的先后次序是___________(填字母)。
a.HCl、BaCl2、AgNO3 b.AgNO3 HNO3、Ba(NO3)2 c. HNO3、Ba(NO3)2、AgNO3 d.AgNO3、HCl、BaCl2
(2)“侯氏制碱法”的原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
如图是某兴趣小组在实验室中模拟“侯氏制碱法”制取NaHCO3所用到的主要装置。

请回答下列问题:
①各仪器口的连接顺序为a接________接b,实验时先向饱和NaCl溶液中通入较多的NH3,再通人足量的CO2,其原因是________(填 写序号字母)。
a.使CO2更易被吸收 b.NH3比CO2更易制取 c.CO2的密度比NH3大
②将生成的NaHCO3晶体从混合物中分离出来需要的玻 璃仪器是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol·L-1NaOH溶液,所加NaOH 溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是( )
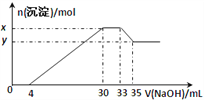
A. x-y=2×10-3mol
B. 原溶液中n(Cu2+)=0.025mol
C. 原溶液的pH=2
D. 原溶液中c(NH4+)=7.5×10-3mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com