
【题目】(17分)A、B、D、E、F为短周期元素,非金属元素A 最外层电子数与其周期数相同,B 的最外层电子数是其所在周期数的2 倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A 在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F 的离子方程式_______。
(2)B、D、E组成的一种盐中,E 的质量分数为43%,其俗名为_____,其水溶液与F单质反应的化学方程式:_______。在产物中加入少量KI,反应后加入CCl4并振荡,有机层显___色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A的二元离子化合物 |
b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
c | 化学组成为BDF2 |
d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为 ;b的化学式为 ;c的电子式为 。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过 键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,这种新能源物质在海底和冰川储童丰富,是巨大的潜在能源。
【答案】(1)第一周期IA族;2Cl-+2H2O![]() 2OH-+H2↑+C12↑(或2NaCl(熔融)
2OH-+H2↑+C12↑(或2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
(2)纯碱(或苏打);2Na2CO3+Cl2+H2O = NaClO+NaCl+2NaHCO3;紫;
(3)NaH;Na2O2和Na2C2; 。
。
(4)氢。
【解析】试题分析:A,B,D,E,F为短周期元素,非金属元素A最外层电子数与其周期数相同,则A为H元素;B的最外层电子数是其所在周期数的2倍,则B为C或S元素,B在D中充分燃烧能生成其最高价化合物BD2,则D为O元素,B的最高正价为+4价,则B为C元素;E+与D2-具有相同的电子数,则E为Na元素;A在F中燃烧,产物溶于水得到一种强酸,则F为Cl元素。(1)已知A为H元素,在周期表中位于第一周期ⅠA族;工业上常用电解饱和食盐水的方法来制备氯气,其电解离子方程式为:2Cl-+2H2O![]() 2OH-+H2↑+C12↑;(2)C、O、Na组成的一种盐中,Na的质量分数为43%,则该物质为碳酸钠,其俗名为纯碱(或苏打);碳酸钠与氯气反应生成氯化钠、次氯酸钠、碳酸氢钠,反应的化学方程式为:2Na2CO3+Cl2+H2O = NaClO+NaCl+2NaHCO3;在反应产物的水溶液中含有强氧化性的NaClO,他可以将I-氧化产生I2,I2容易溶于有机物,而在水中溶解度较小,所以得到的I2的CCl4溶液显紫色;(3)这几种元素只有Na能与H形成离子化合物,则a的化学式为NaH;含有非极性共价键的二元离子化合物,且原子数之比为1:1,则b为Na2O2和Na2C2;c化学组成为BDF2,该物质的分子式是COCl2, COCl2结构式为
2OH-+H2↑+C12↑;(2)C、O、Na组成的一种盐中,Na的质量分数为43%,则该物质为碳酸钠,其俗名为纯碱(或苏打);碳酸钠与氯气反应生成氯化钠、次氯酸钠、碳酸氢钠,反应的化学方程式为:2Na2CO3+Cl2+H2O = NaClO+NaCl+2NaHCO3;在反应产物的水溶液中含有强氧化性的NaClO,他可以将I-氧化产生I2,I2容易溶于有机物,而在水中溶解度较小,所以得到的I2的CCl4溶液显紫色;(3)这几种元素只有Na能与H形成离子化合物,则a的化学式为NaH;含有非极性共价键的二元离子化合物,且原子数之比为1:1,则b为Na2O2和Na2C2;c化学组成为BDF2,该物质的分子式是COCl2, COCl2结构式为![]() ,则其电子式为
,则其电子式为 ;只存在一种类型作用力且可导电的单质晶体为Na,Na属于金属晶体;(4)由A和B元素组成的二元化合物是沼气的主要成分,为CH4,A、C形成的化合物是H2O,水分子之间形成氢键,甲烷分子空间构性是正四面体结构。会进入水分子之间形成的空腔内,形成甲烷的水合物,得到可燃冰。
;只存在一种类型作用力且可导电的单质晶体为Na,Na属于金属晶体;(4)由A和B元素组成的二元化合物是沼气的主要成分,为CH4,A、C形成的化合物是H2O,水分子之间形成氢键,甲烷分子空间构性是正四面体结构。会进入水分子之间形成的空腔内,形成甲烷的水合物,得到可燃冰。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】明朝《菽园杂记》有海水提取食盐的记载:“烧草为灰,布在滩场,然后以海水渍之,侯晒结浮白,扫而复淋”。该过程中“灰”的作用是( )
A. 萃取 B. 吸附 C. 结晶 D. 蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组拟对一种焰火原料(由两种短周期的常见金属单质Li,Na,Mg,Al组成的合金粉末)进行探究.请完成下列探究报告.
【探究目的】探究该焰火原料的组成
【资料检索】①Mg2+检验方法:取2滴待检液,加入2滴2molL﹣1NaOH溶液,再加入1滴镁试剂(Ⅰ)染料(对硝基苯偶氮苯二酚).若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待检液中含有Mg2+.但Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+检出
②Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶碱难溶于氯化铵
③很多合金是金属互化物,有确定的化学组成
【探究思路】①确定焰火原料所含金属种类;②测定焰火原料的化学式
【实验探究】(1)甲同学进行了初步试验,实验步骤和实验现象如下.请填写下表.
试验序号 | 实 验 步 骤 | 实 验 现 象 | 结 论 |
① | 取少量该焰火原料加入冷水 | 无明显现象 |
|
② | 取少量该焰火原料加入稀盐酸 | 完全溶解,有大量气体产生,溶液呈无色 |
|
(2)乙同学取甲第②组实验的溶液,加入镁试剂(Ⅰ)染料,得出合金中不含镁.乙的结论 (选填“正确”或“错误”),你的理由是 .
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下.
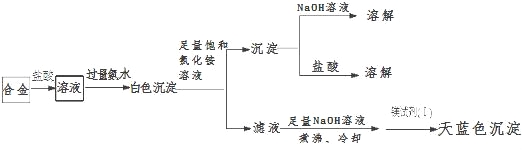
由丙的实验记录可知,该焰火原料是由 和 两种金属组成的合金;实验中滤液加入足量氢氧化钠溶液后需煮沸,煮沸的理由是 .
(4)丁同学利用丙同学的结论,设计如下图所示的实验步骤,确定合金组成.

问题讨论:
①能确定合金组成的数据组有 (填写选项字母);
A.m、n B.m、y C.n、y
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,试在右图中作出y随x变化的曲线;

③当y=8.5mol时,该合金是一种金属互化物,其化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C![]() 2AlN+3CO,下列叙述正确的是( )
2AlN+3CO,下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体,熔点和沸点较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某些化学知识用数轴表示,可以收到直观、简明、易记的效果。用数轴表示的下列知识正确的是( )
A. 硫及其化合物的化合价与氧化还原反应的关系:
B. 分散系的分类:
C. AlCl3溶液与NaOH溶液反应后铝元素的存在形式:
D. CO2与NaOH溶液反应后的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题12分)如图是元素周期表的框架,请在表中①~⑩元素中回答问题

请用化学语言回答下列问题:
(1)在表中④、⑤、⑥三种元素的简单离子半径由大到小的顺序为______。
(2)其中⑤与⑦两元素的最高价氧化物的水化物反应的离子方程式为______。
(3)⑧与⑩两种元素非金属较强的是______,请用一个离子方程式证明该结论______。
(4)①与③的两种单质可以在金属铂做电极时构成一种对环境友好的燃料电池,电解质为⑨的最高价氧化物的水化物,请书写出正极反应式______,电池工作时阴离子定向移动到______极(填正或负)。
(5)元素①与⑧的两种单质在一定条件下可反应生成一种化合物甲,已知下表中的数据是破坏1mol物质中的化学键所吸收的能量(kJ),则生成1mol甲时释放的能量为______kJ。
化学键 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.5L的AlCl3溶液中逐滴加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果正确的是( )

A.反应过程中,沉淀最多时的质量为7.8g
B.AlCl3溶液的浓度为2.0 molL﹣1
C.得到39g沉淀时,消耗的NaOH溶液体积一定为1.5 L
D.当V(NaOH)=4.0 L时,得到的溶液中含Na+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素按最高正价递增顺序排列的是
A. N、O、F、Ne B. Li、Be、B、C
C. Li、Na、Be、Mg D. F、Cl、Br、I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。其方法与分离下列物质的实验方法原理上相同的是
A. 甲苯和水 B. 硝酸钾和氯化钠
C. 食盐水和泥沙 D. 乙酸乙酯和甘油(丙三醇)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com