
| A. | 蒸发时将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 | |
| D. | 向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+ |
分析 A.蒸发皿是可以直接加热的仪器,不需要垫上石棉网;
B.萃取剂的密度可以比水小,如苯;
C.氧化铝的熔点较高,包裹在铝表面,导致Al加热熔化但不滴落;
D.由于红褐色能够掩盖白色,无法判断是否含有镁离子.
解答 解:A.蒸发时将蒸发皿放置在铁架台的铁圈上,可以直接加热,不需要加垫石棉网,故A错误;
B.萃取操作时,萃取剂与原溶剂必须互不相溶,萃取剂的密度不一定比水大,如有机溶剂苯的密度小于水,故B错误;
C.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝,故C正确;
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明该溶液中含有Fe2+,由于氢氧化镁白色沉淀易被红褐色掩盖,则无法确定原溶液中是否含有Mg2+,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高考的高频题,题目难度中等,涉及蒸发、萃取、铝、铁及化合物性质等知识,明确常见化学实验基本操作方法为解答关键,注意熟练掌握常见元素及其化合物性质,试题培养了学生的分析能力及化学实验能力.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:解答题
| 化学式 | Cl2O | ClO2 | Cl2O7 |
| 沸点/℃ | 3.8 | 11.0 | 82.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 步骤①、③的操作都是过滤 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤③中加入的有机溶剂是乙醇 | |
| D. | 步骤④的操作是精馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
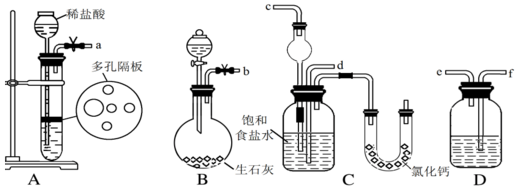
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
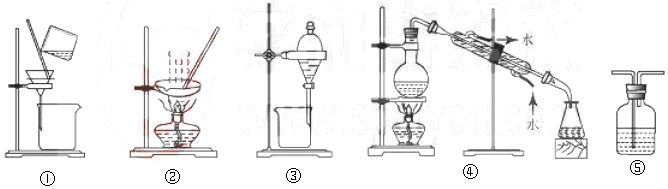
| A. | 粗盐提纯,选①和② | B. | 用CC14提取碘水中的碘,选③ | ||
| C. | 用NaOH溶液吸收少量C12选⑤ | D. | 分离Na2CO3溶液和CH3COOC2H5,选④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 min内,Y的平均反应速率为0.03 mol•L-1•s-1 | |
| B. | 10 min内,X和Y反应放出的热量为a kJ | |
| C. | 10 min内,消耗0.2 mol X,生成0.4 mol Z | |
| D. | 10 min内,前5minX的平均反应速率与后5minX的平均反应速率相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m=53 c2=a/b | B. | m=-26.5 2c=a-b | C. | m=-170.5 2c=a-b | D. | m=26.5 c2=$\frac{a}{b}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
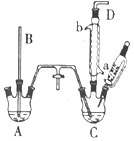 氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下:
氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下: +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$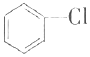 +HCl
+HCl查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com