
| A、从组成看,其成分皆是碱性氧化物 |
| B、溶液Y中的阳离子主要是Mg2+、Al3+、Fe2+、H+ |
| C、沉淀X的成分是SiO2 |
| D、在溶液Y中加入过量的氨水,过滤得到的沉淀的成分是Fe(OH)3和Mg(OH)2 |


科目:高中化学 来源: 题型:
| ||
| ||
| ||

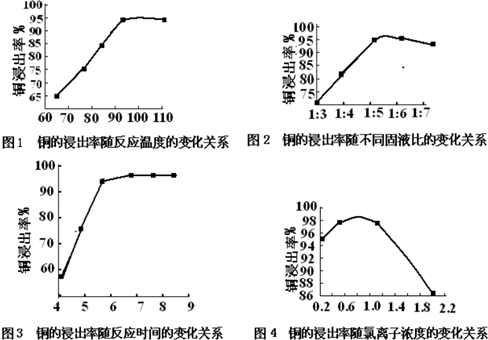
| 选项 | 反应温度/℃ | 固液比 | c(Cl-)/mol?L-1 | 反应时间/h |
| a | 100 | 1:5.5 | 0.7 | 7 |
| b | 95 | 1:5 | 0.8 | 6 |
| c | 110 | 1:6 | 0.9 | 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
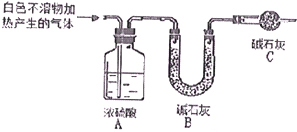 某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.
某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH(aq) |
| △ |
| CO2 |
| O2/点燃 |
| H2O |
| Ag |
| HCl(aq) |
| △ |
| 石灰乳 |
| 煅烧 |
| O2 |
| O2,H2O |
| A、①②③④ | B、①③④⑥ |
| C、①③⑤⑥ | D、②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在一定条件下能分解为SO2和O2 |
| B、是硫酸的酸酐 |
| C、其中硫元素已不能再被氧化 |
| D、取8g SO3溶于92g水中得8%溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
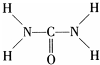 尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.
尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com