
| A. | 与煤相比,天然气是较清洁的化石燃料 | |
| B. | 煤的干馏和石油的分馏都是物理变化 | |
| C. | 煤燃烧产生的硫氧化物和氮氧化物是形成酸雨的主要物质 | |
| D. | 苯可从煤焦油中提取,它是广泛应用的化工原料,有特殊气味,有毒 |
分析 A.煤中含有硫氮等元素;
B.煤的干馏是将煤隔绝空气加强热使其分解生成煤焦油、煤气、焦炭等新物质的过程;
C.煤燃烧产生的硫氧化物和氮氧化物是形成硝酸型、硫酸型酸雨的原因;
D.苯是广泛应用的化工原料,有特殊气味,有毒.
解答 解:A.煤中含有硫氮等元素,天然气的主要成分是甲烷,故A正确;
B.煤的干馏是将煤隔绝空气加强热使其分解生成煤焦油、煤气、焦炭等新物质的过程,该过程中有新物质生成,属于化学变化,故B错误;
C.煤燃烧产生的硫氧化物和氮氧化物是形成硝酸型、硫酸型酸雨的原因,故C正确;
D.从煤焦油中提取可以提取苯,苯是广泛应用的化工原料,有特殊气味,有毒,故D正确.
故选B.
点评 本题考查清洁能源、物理变化与化学变化的区别、酸雨的成因等知识,难度不大,注意苯是有毒的化工原料.


 培优口算题卡系列答案
培优口算题卡系列答案科目:高中化学 来源: 题型:解答题
| 化学键 | C-H | C-F | H-F | F-F | H-H | H-N |
| 键 能 | 414 | 489 | 565 | 158 | 436 | 391 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
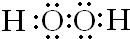 ,E离子的电子排布式为1s22s22p6,B原子的电子排布图为
,E离子的电子排布式为1s22s22p6,B原子的电子排布图为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
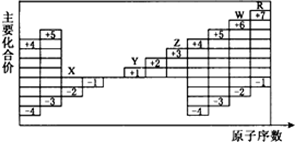
| A. | 五种元素中有三种属于非金属元素,且三种非金属元素均存在同素异形现象 | |
| B. | 五种元素中有两种属于金属元素,且两种金属元素均不能在空气中稳定存在 | |
| C. | 五种元素的单质在固态时分别属于三种不同的晶体类型 | |
| D. | Y、Z、W三种元素的最高价氧化物的水化物相互之间均能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度 | B. | 增大铁片的质量 | ||
| C. | 用铁粉代替铁片 | D. | 用98%的浓硫酸替代稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
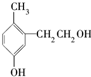
| A. | 它是苯酚的同系物 | |
| B. | 1mol该有机物能与2 mol溴水发生取代反应 | |
| C. | 1mol该有机物能与金属钠反应产生0.5 mol H2 | |
| D. | 1mol该有机物能与2 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 598 | B. | 576 | C. | 288 | D. | 299 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将食物保存在电冰箱里 | |
| B. | 做粉尘爆炸实验时选用很细的面粉 | |
| C. | 向过氧化氢溶液中加入MnO2 | |
| D. | 铁与稀盐酸反应太慢时加入较浓的盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com