
在2 L密闭容器内,800℃时NO(g)和O2(g)反应生成NO2(g)的体系中,n(NO)随时间的变化如表所示:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应,在第5 s时,NO的转化率为________。
(2)下图中表示NO2变化曲线的是________,用O2表示从0~2 s内该反应的平均速率v=________。

(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
解析 (1)该反应是可逆反应,5 s时,NO转化率为: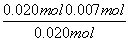 ×100%=65%。
×100%=65%。
(2)由平衡体系2NO(g)+O2(g)2NO2(g)知,NO2为生成物,初始状态时,c(NO2)=0,随反应的进行,c(NO2)逐渐增大,当达到平衡时,c(NO2)= -
- =0.006 5 mol/L,故表示NO2变化曲线的为b。
=0.006 5 mol/L,故表示NO2变化曲线的为b。
v(NO)= =
= =
= =0.003 mol/(L·s),
=0.003 mol/(L·s),
则v(O2)= v(NO)=0.001 5 mol/(L·s)。
v(NO)=0.001 5 mol/(L·s)。
(3)a项中未指明正、逆反应速率,故无法说明该反应是否达到平衡状态;由于该反应是前后气体体积不相等的反应,当容器内压强保持不变时,说明该反应已达到平衡状态,故b项正确;c项中已说明正、逆反应速率相等,故说明该反应已达到平衡状态;由于气体总质量不变,气体总体积也不变,因此,无论该反应是否达到平衡,容器内气体密度总保持不变,故d项无法说明该反应是否达到平衡状态。
答案 (1)是 65% (2)b 0.001 5 mol/(L·s) (3)bc


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
下列各组物质中化学键的类型相同的是( )
A.H2SO4、MgCl2、NH4Br
B.HF、Na2O、CO
C.H2O、C2H4、CO2
D.CaCl2、NaOH、SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可表示为:2Ag+Zn(OH)2充电放电Ag2O+Zn+H2O,在此电池放电时,负极上发生反应的物质是( )
A.Ag B.Zn(OH)2
C.Ag2O D.Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )

A.反应的化学方程式为:2MN
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应:X2(g)+Y2(g)2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L,在一定的条件下,当反应达到平衡时,各物质浓度有可能是( )
A.Z为0.3 mol/L B.Y2为0.35 mol/
C.X2为0.2 mol/L D.Z为0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A+2B===3C+2D,在不同条件下的反应速率如下,其中最快的是( )
A.v(A)=0.3 mol·(L·s)-1
B.v(B)=0.9 mol·(L·s)-1
C.v(C)=0.6 mol·(L·s)-1
D.v(D)=0.8 mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:

加入0.1 mol MnO2粉末于50 mL一定浓度的过氧化氢溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。
(1)实验时放出气体的总体积是________。
(2)放出 气体所需时间为________。
气体所需时间为________。
(3)反应放出 气体所需时间约为________。
气体所需时间约为________。
(4)A、B、C、D各点反应速率快慢的顺序为_______________。
(5)解释反应速率变化的原因:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

如右图所示,把试管放入盛有25 ℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴加5 mL盐酸于试管中。试回答下列问题:
(1)实验中观察到的现象是______________________________。
(2)产生上述现象的原因是______________________________。
(3)写出有关反应的离子方程式:_______________________。
(4)由实验推知,镁片和盐酸的总能量________(填“大于”“小于”或“等于”)氯化镁溶液和氢气的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,我国科学家对有机物自由基的研究有新的突破,在国际上占有领先的地位。有机物中常见的最简单的自由基是碳烯(· H2),它十分活泼,很容易用它的未成对电子与不饱和烃反应,生成三碳环;也可以插在烷基的碳氢键(C—H)之间,使碳链增长。请回答下列问题。
H2),它十分活泼,很容易用它的未成对电子与不饱和烃反应,生成三碳环;也可以插在烷基的碳氢键(C—H)之间,使碳链增长。请回答下列问题。
(1)写出碳烯的电子式:________。
(2)写出碳烯与丙烯反应产物的结构简式:____________。
(3)碳烯与烃A反应,生成烃B,一定量的B完全燃烧生成4.4 g CO2和2.25 g H2O,B分子中含有3个—CH3,写出B的结构简式:
_________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com