
【题目】下列应用不涉及氧化还原反应的是
A. Na2O2用作呼吸面具的供氧剂 B. 工业上电解熔融状态Al2O3制备Al
C. 工业上利用合成氨实现人工固氮 D. 实验室用NH4Cl 和Ca(OH)2制备NH3
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
【题目】常温下,将20.0g质量分数为14.0%的KNO3溶液跟30.0g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15g·cm-3的混合溶液。计算:
(1)混合后溶液的质量分数___________。
(2)混合后溶液的物质的量浓度_____________。
(3)在1000g水中需溶解_____________摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。

①在图示的转化中,化合价不变的元素是_________________。
②反应中当有1mol H2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需消耗O2的物质的量为_________________。
(2)已知硫有多种同素异形体,如S2 、S4、 S6 、S8等。H2S在高温下分解生成硫蒸气和H2。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示,H2S在高温下分解反应的化学方程式为_______________________。

(3)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题20图- 1和题20图- 2所示。

(3)溶液的pH对吸附剂X表面所带电荷有影响。pH =7. 1时, 吸附剂X表面不带电荷; pH > 7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多。pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如题20图-3所示。

①在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,其原因是____________。
②在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,这是因为___________。 提高吸附剂X对三价砷去除效果可采取的措施是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列反应事实写出相应的化学方程式。
(1)双氧水在二氧化锰的催化作用下生成水和氧气:____________。
(2)在尘埃的作用下,二氧化硫和氧气反应生成三氧化硫(SO3):___________。
(3)Cu和AgNO3溶液反应,生成Cu(NO3)2溶液和Ag:_____________。
(4)少量CuSO4溶液滴入NaOH稀溶液中生成Cu(OH)2沉淀和Na2SO4溶液:____________。
(5)一氧化碳和四氧化三铁(Fe3O4)在高温下反应,生成铁和二氧化碳:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 若反应2A(S)+B(g)![]() 2C(g)ΔH>0 能自发进行,原因是ΔS<0
2C(g)ΔH>0 能自发进行,原因是ΔS<0
B. 催化剂能改变反应的途径,但不能改变反应的ΔH
C. S(g)+O2(g)===SO2(g) ΔH1<0; S(s)+O2(g)===SO2(g) ΔH2<0,则ΔH1>ΔH2。
D. 化学平衡CO(g)+H2O(g)![]() CO2(g)+H2(g),增加H2O的浓度H2O的转化率增大
CO2(g)+H2(g),增加H2O的浓度H2O的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】家用液化气的主要成分为丙烷、丙烯、丁烷和丁烯,下列说法不正确的是( )
A. 丙烯和丁烯均能发生加成反应 B. 可用溴水来鉴别丙烷与丙烯
C. 丁烷中所有原子不可能处于同一平面 D. 丙烷的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于皂化反应的是
A. 乙酸乙酯在碱性条件下水解 B. 硬脂酸甘油酯在酸性条件下水解
C. 软脂酸甘油酯在酸性条件下水解 D. 硬脂酸甘油酯在碱性条件下水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】荧光棒的发光原理是利用过氧化氢氧化某草酸二酯产生能量传递给荧光物质发出荧光。该草酸二酯的结构简式如下图所示。下列有关该草酸二酯的说法不正确的是
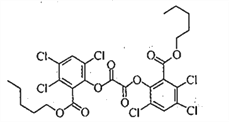
A. 分子中含有一种含氧官能团
B. 苯环上的一溴代物只有一种
C. 可以发生取代反应和加成反应
D. lmol草酸二酯与NaOH溶液反应最多消耗4mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲:![]() 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
乙:![]() 无色,无气味并且易燃。是常见的一种基础能源。
无色,无气味并且易燃。是常见的一种基础能源。
丙:![]() 有强氧化性的弱酸,可以用于消毒杀菌。
有强氧化性的弱酸,可以用于消毒杀菌。
请根据上述信息回答下列问题。
(1)B元素在元素周期表中的位置为________________,请写出BC2分子的电子式:_______________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:_____________________________________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生反应:______________________________________________________。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液。滴加过程中的现象为:
①试管中溶液变成深棕黄色,发生反应的离子方程式为 ;
②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀。请回答“片刻后反应变得剧烈”的原因是a b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com