
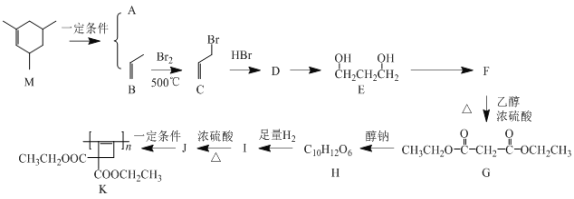
【题目】由原料M合成高分子K的某种合成路线如图:
已知:
①![]()
②![]() +HO—R’
+HO—R’
③H2C=C=CH2结构不稳定,将转化为HC![]() C—CH3
C—CH3
(1)A的系统命名为___。
(2)由D生成E过程的化学方程式为___。
(3)由G生成H过程的反应类型为___。
(4)I的结构简式为___。
(5)J中所含官能团名称为___。
(6)X是比M分子量少14的同系物,则具有下列条件的X的结构有___种。
①含有六元环
②能使溴水褪色
(7)利用上述流程的相关信息及所学知识,设计流程,由乙醇合成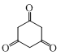 ___。
___。
【答案】2—甲基—1,3—戊二烯 BrCH2CH2CH2Br+2NaOH![]() HOCH2CH2CH2OH+2NaBr 取代反应
HOCH2CH2CH2OH+2NaBr 取代反应 ![]() 碳碳三键、酯基 19 CH3CH2OH
碳碳三键、酯基 19 CH3CH2OH![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3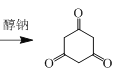
【解析】
根据框图可知,化合物M(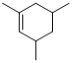 )开环生成A(
)开环生成A(![]() )和B(
)和B(![]() ),B与Br2发生取代反应生成C(
),B与Br2发生取代反应生成C(![]() ),C与HBr发生加成反应生成D(
),C与HBr发生加成反应生成D(![]() ),D发生水解反应生成E(
),D发生水解反应生成E(![]() ),E发生氧化反应生成F(
),E发生氧化反应生成F(![]() ),F与乙醇发生酯化反应生成G(
),F与乙醇发生酯化反应生成G(![]() ),G在醇钠的作用下发生取代反应生成H(
),G在醇钠的作用下发生取代反应生成H( ),H与足量氢气发生加成(或还原)反应生成I(
),H与足量氢气发生加成(或还原)反应生成I( ),I在浓硫酸的作用下发生消去反应生成同碳二烯,该物质不稳定转化为J(
),I在浓硫酸的作用下发生消去反应生成同碳二烯,该物质不稳定转化为J(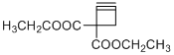 ),J发生加聚反应生成最终产物K。
),J发生加聚反应生成最终产物K。
(1)根据分析,A的键线式为![]() ,系统命名为2—甲基—1,3—戊二烯;
,系统命名为2—甲基—1,3—戊二烯;
(2)根据分析,由D生成E是卤代烃的水解反应,化学方程式为BrCH2CH2CH2Br+2NaOH![]() HOCH2CH2CH2OH+2NaBr;
HOCH2CH2CH2OH+2NaBr;
(3)根据分析,由G生成H过程的反应类型为取代反应;
(4)根据分析,I的结构简式为 ;
;
(5)根据分析,J为 ,官能团有碳碳三键和酯基;
,官能团有碳碳三键和酯基;
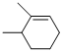
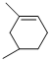
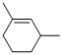
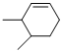
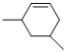
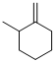
(6)X是比M分子量少14的同系物,说明X分子式为C8H14,能使溴水褪色说明X有碳碳双键,含有六元环的同分异构体有![]() 、
、![]() 、
、![]() 、
、![]() 、
、 、
、 、
、 、
、![]() 、
、 、
、![]() 、
、 、
、 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、 、
、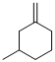 、
、![]() 共19种;
共19种;
(7)由乙醇合成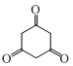 可用有机合成的逆推法,
可用有机合成的逆推法, 可用已知②中的方法,用CH3COOCH2CH3和醇钠制得,乙酸乙酯由乙醇和乙酸发生酯化反应制得,乙酸可由乙醇氧化制得,故反应路线为:
可用已知②中的方法,用CH3COOCH2CH3和醇钠制得,乙酸乙酯由乙醇和乙酸发生酯化反应制得,乙酸可由乙醇氧化制得,故反应路线为:
CH3CH2OH![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3 ;
;


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
【题目】2020年我国废旧锂离子电池的产生将达到爆发期,某高校实验室利用废旧钴酸锂正极片进行钴酸锂的再生工艺设计如下,请回答下列问题:
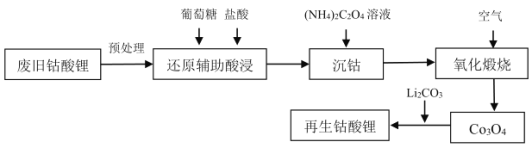
(1)拆解废旧电池前需要进行放电,以避免在拆解过程中因局部短路起火,放电方式为电化学放电,可以将废旧电池浸泡在_____________中进行放电。
A.酒精 B.98%H2SO4C.Na2SO4溶液
(2)预处理时,钴酸锂(Li0.5CoO2)高温下分解得到LiCoO2、Co3O4和一种气体,该反应的化学方程式为_________________。
(3)已知难溶物CoC2O4的Ksp=4.0×10-6,一般认为离子浓度达到10-5mol/L时即完全除尽。沉钴过程中,当Co2+完全沉淀时,溶液中![]() 的浓度至少为_________mol/L。
的浓度至少为_________mol/L。
(4)沉钴过程中,草酸盐体系中钴离子形态分布如图,在不同pH范围钴离子形态不同的原因___________________。

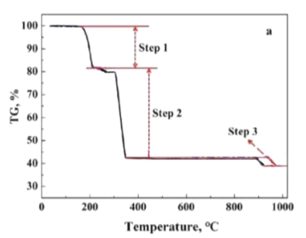
(5)在空气氛围下CoC2O42H2O氧化分解制备Co3O4的失重曲线如图所示,已知![]() 失重率大约为19.7%;
失重率大约为19.7%;![]() 失重率大约为36.3%;
失重率大约为36.3%;![]() 失重率大约为3.0%。请写出
失重率大约为3.0%。请写出![]() 发生的化学反应方程式______________________。
发生的化学反应方程式______________________。
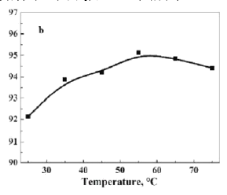
(6)已知生成草酸钴的过程为吸热过程。在![]() ,沉淀时间
,沉淀时间![]() ,考察温度对Co2+沉淀率的影响,结果如图所示,沉淀率呈先增大后减小的趋势的原因可能____________。
,考察温度对Co2+沉淀率的影响,结果如图所示,沉淀率呈先增大后减小的趋势的原因可能____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然油脂的分子式为C57H106O6。1 mol该油脂水解可得到1 mol甘油、1 mol脂肪酸X和2 mol直链脂肪酸Y。经测定X的相对分子质量为280,原子个数比为C∶H∶O=9∶16∶1。下列说法错误的是( )
A.X的分子式为C18H32O2
B.脂肪酸Y能发生取代反应
C.Y的结构简式可能为CH3CH=CH(CH2)14COOH
D.Y的结构简式为CH3(CH2)16COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C-C可以绕键轴旋转,结构简式为下图的烃,下列说法正确的是:
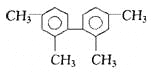
A.分子中至少有9个碳原子处于同一平面上
B.分子中至少有11个碳原子处于同一平面上
C.该烃的一氯取代物最多有3种
D.该烃是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016 年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB 族元素对应离子的萃取,如La3+、Sc2+。写出基态二价 钪离子(Sc2+)的核外电子排布式:____,其中电子占据的轨道数为_____个。
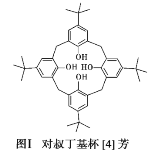
(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为_____,羟基间的相互作用力为_____。
(3)不同大小苯芳烃能识别某些离子,如:N3-、SCN等。一定条件下,SCN与 MnO2反应可得到(SCN)2,试写出(SCN)2的结构式_______。
(4)NH3分子在独立存在时 H-N-H 键角为 106.7°。 [Zn(NH3)6]2+离子中 H-N-H 键角变为 109.5°,其原因是:_________________________。
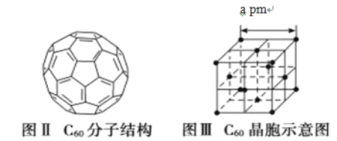
(5)已知 C60 分子结构和 C60 晶胞示意图(如图Ⅱ、图Ⅲ所示):则一个 C60 分子中含有σ键的个数为______,C60 晶体密度的计算式为____gcm3。(NA 为阿伏伽德罗常数 的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物G是4-羟基香豆素,是重要的医药中间体,可用来制备抗凝血药,可通过下列路线合成。
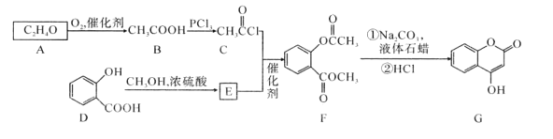
请回答:
(1)D→E的反应类型是___。
(2)G中含有的官能团名称为____。
(3)写出G和过量NaOH溶液共热时反应的化学方程式___。
(4)化合物E的同分异构体很多,符合下列条件的结构共___种。
①能与氯化铁溶液发生显色反应;②能发生银镜反应;③能发生水解反应
其中,核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的结构简式为____。
(5)E的同分异构体很多,所有同分异构体在下列某种表征仪器中显示的信号(或数据)完全相同,该仪器是___(填标号)。
a.质谱仪 b.元素分析仪 c.红外光谱仪 d.核磁共振仪
(6)已知酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯(![]() )是一种重要的有机合成中间体。请根据已有知识并结合相关信息,试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选):___。
)是一种重要的有机合成中间体。请根据已有知识并结合相关信息,试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选):___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①一个N≡N断裂的同时,有3个H—H键断裂
②一个N≡N键断裂的同时,有6个N—H键断裂
③其它条件不变时,混合气体平均相对分子质量不再改变
④恒温恒容时,体系压强不再改变
⑤NH3、N2、H2的体积分数都不再改变
⑥恒温恒容时,混合气体的密度保持不变
⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min)
A.全部B.①③④⑤C.②③④⑤⑦D.③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A. 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为(7/22.4)NA
B. 1 mol甲基(-CH3)所含的电子总数为9NA
C. 0.5 mol1,3-丁二烯分子中含有碳碳双键数为NA
D. 1 mol碳正离子(CH3+)所含的电子总数为8NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com