
| A、标准状况下,H2和O2各11.2L相混合,混合气体所含分子总数为NA |
| B、1.8g的NH4+中,所含电子总数为NA |
| C、7g乙烯和丙烯的混合物中,所含原子总数为NA |
| D、1 mol?L-1的NaOH溶液中,所含Na+总数为NA |
| 1.8g |
| 18g/mol |
| 7g |
| 14g/mol |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| A、0.1 mol NH4+中含有3NA个共价单键 |
| B、标准状况下,11.2L臭氧中含有NA个氧原子 |
| C、2gH218O中含有NA个中子 |
| D、84gNaHCO3溶于水,溶液中含有NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
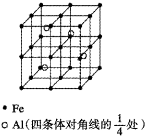 组成蛋白质的元素主要有C、H、O、N及S、P和少量的Zn、Cu、Fe等.
组成蛋白质的元素主要有C、H、O、N及S、P和少量的Zn、Cu、Fe等.| 共价键 | C-C | C-N | C-S |
| 键能/kJ?mol-1 | 347 | 305 | 259 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 [化学一物质结构与性质]
[化学一物质结构与性质]查看答案和解析>>
科目:高中化学 来源: 题型:
| 相关实验 | 预期目的 | |
| A | 相同温度下,等质量的大理石块、大理石粉分别与等体积、等浓度的盐酸反应 | 探究接触面积对化学反应速率的影响 |
| B | 把装有颜色相同的NO2和N2O4混合气的两支试管(密封)分别浸入冷水和热水中 | 探究温度对化学平衡的影响 |
| C | 在蔗糖中加入稀硫酸,水浴加热,再加入新制的氢氧化铜并加热 | 探究蔗糖水解产物具有还原性 |
| D | 两支试管中装有等体积、等浓度H2O2溶液,向其中一支试管中加入MnO2固体 | 探究MnO2固体对H2O2分解速率的影响 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,1mol甲基(-CH3)所含电子数为7NA |
| B、0.4 mol以任意比例混合的乙炔和乙醛气体充分燃烧时,消耗氧气分子数为NA |
| C、常温常压下,NA个甲烷分子的体积大于22.4 L |
| D、1 mol Na2O2与水反应,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 目标生成物的质量 |
| 参加该反应所有反应物的总质量 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol甲醛分子中含C-H键数目为2NA |
| B、常温常压下,7g乙烯分子的数目为0.5NA |
| C、25℃,pH=2的盐酸中含有H+的数目为0.01NA |
| D、标准状况下,2.24L氯气与1.12L液态水反应转移的电子数一定为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com