
| 序号 | 烧杯中的液体 | 5分钟后现象 |
| ① | 2mL 1mol•L-1KI溶液+5滴淀粉 | 无明显变化 |
| ② | 2mL1mol•L-1KI 溶液+5 滴淀粉+2mL0.2mol•L-1HC1 | 溶液变蓝 |
| ③ | 2mLl mol•L-1KI溶液+5滴淀粉+2mL0.2mol•L-1KC1 | 无明显变化 |
| ④ | 2mL1mol•L-1KI溶液+5滴淀粉+2mL0.2mol•L-1CH3COOH | 溶液变蓝,颜色 较②浅 |
| 序号 | 烧杯中的液体 | 5小时后现象 |
| ⑤ | 2mL混有KOH的pH=8.5的lmol•L-1KI溶液+5滴淀粉 | 溶液略变蓝 |
| ⑥ | 2mL混有KOH的pH=10的lmol•L-1KI溶液+5滴淀粉 | 无明显变化 |
分析 (1)对比实验①②③可知实验目的是验证碘化钾被氧气氧化的条件和影响离子;
(2)2mL1mol•L-1KI 溶液+5 滴淀粉+2mL0.2mol•L-1HC1,溶液变蓝色,说明碘离子被氧化为碘单质;
(3)对比②④盐酸和醋酸相比,醋酸是弱酸氢离子浓度小;
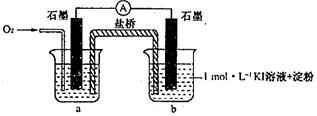
(4)实验⑤2mL混有KOH的pH=8.5的lmol•L-1KI溶液+5滴淀粉溶液略变蓝,2mL混有KOH的pH=10的lmol•L-1KI溶液+5滴淀粉无明显变化,甲同学猜想“pH=10时O2不能氧化I-”,实验验证利用原电池原理判断,烧杯a中是pH=10的氢氧化钾溶液;
(5)若pH=10时O2不能氧化I-,通入O2后能发生原电池反应,b中淀粉变蓝色;
(6)pH=10的“KOH一淀粉溶液”中滴加碘水,溶液先变蓝后迅速褪色,经检测褪色后的溶液中含有IO3-,是碘单质和碱反应生成碘酸钾和碘化钾和水;
(7)中性条件下,O2的氧化性比较弱,短时间内难以生成“一定量”碘单质使溶液颜色发生变化,pH=10的KOH溶液中I-被氧化生成I2,碘单质迅速和碱发生气化反应.
解答 解:(1)2mL 1mol•L-1KI溶液+5滴淀粉无变化,2mL1mol•L-1KI 溶液+5 滴淀粉+2mL0.2mol•L-1HC1,溶液变蓝色,说明碘离子被氧化为碘单质,2mLl mol•L-1KI溶液+5滴淀粉+2mL0.2mol•L-1KC1无变化,比较可知氢离子影响碘化钾中碘离子被空气氧化,实验③的目的是验证Cl-是否影响KI与O2的反应,
故答案为:验证Cl-是否影响KI与O2的反应;
(2)2mL1mol•L-1KI 溶液+5 滴淀粉+2mL0.2mol•L-1HC1,溶液变蓝色,说明碘离子被氧化为碘单质,反应的离子方程式为:4I-+O2+4H+=2I2+2H2O,
故答案为:4I-+O2+4H+=2I2+2H2O;
(3)2mL1mol•L-1KI 溶液+5 滴淀粉+2mL0.2mol•L-1HC1,溶液变蓝,2mL1mol•L-1KI溶液+5滴淀粉+2mL0.2mol•L-1CH3COOH,溶液变蓝,颜色较②浅,说明氢离子浓度大小影响氧气氧化碘离子被氧化的测定,实验②比实验④溶液颜色深的原因是其他条件相同时,HCl是强电解质,溶液中c(H+)较醋酸大,O2的氧化性较强,
故答案为:其他条件相同时,HCl是强电解质,溶液中c(H+)较醋酸大,O2的氧化性较强;
(4)实验⑤2mL混有KOH的pH=8.5的lmol•L-1KI溶液+5滴淀粉溶液略变蓝,2mL混有KOH的pH=10的lmol•L-1KI溶液+5滴淀粉无明显变化,甲同学猜想“pH=10时O2不能氧化I-”,实验验证利用原电池原理判断,烧杯a中是pH=10的氢氧化钾溶液,用来验证滴入碘化钾淀粉不变蓝色,
故答案为:pH=10的KOH溶液;
(5)实验结果表明此猜想不成立.支持该结论的实验现象是:通入O2后,电流表指针偏转,烧杯b中的溶液逐渐变蓝色,
故答案为:电流表指针偏转,烧杯b中的溶液逐渐变蓝色;
(6)乙同学向pH=10的“KOH一淀粉溶液”中滴加碘水,溶液先变蓝后迅速褪色,经检测褪色后的溶液中含有IO3-,褪色原因涉及的离子方程式为:3I2+6OH-=IO3-+5I-+3H2O,
故答案为:3I2+6OH-=IO3-+5I-+3H2O;
(7)中性条件下,O2的氧化性比较弱,短时间内难以生成“一定量”碘单质使溶液颜色发生变化,pH=10的KOH溶液中I-被氧化生成I2,碘单质迅速和碱发生气化反应,实验①和实验⑥的现象产生的原因分别可能是:中性条件下,O2的氧化性比较弱,短时间内难以生成“一定量”碘单质使溶液颜色发生变化;pH=10的KOH溶液中I-被氧化生成I2,I2迅速发生歧化反应变为IO3-和I-,
故答案为:中性条件下,O2的氧化性比较弱,短时间内难以生成“一定量”碘单质使溶液颜色发生变化;pH=10的KOH溶液中I-被氧化生成I2,I2迅速发生歧化反应变为IO3-和I-.
点评 本题考查了物质性质、物质反应和现象、实验方案设计、主要是反应现象和影响因素的理解应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
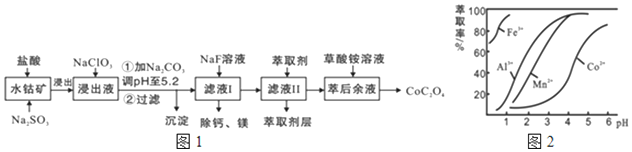
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的PH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量乙酸与碳酸钠溶液反应:2 CH3COOH+CO32-→2CH3COO-+CO2↑+H2O | |
| B. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 乙醛溶液与足量的银氨溶液共热CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | SF6中所有原子均满足8电子稳定结构 | |
| D. | SiF4和SO32-的中心原子均为印sp3杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li在氧气中燃烧主要生成Li2O2 | |
| B. | 碱金属元素单质都能保存于煤油中 | |
| C. | 卤族元素单质的熔、沸点随原子序数的增大而升高而碱金属元素单质的熔、沸点随原子序数的增大而降低 | |
| D. | 第二周期非金属元素的气态氢化物溶于水后所得水溶液均呈酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com