
【题目】在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3,铜粉可溶解的是
A. ①② B. ②④ C. ②③ D. ①④
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】 按系统命名,有机物CH3CH(C2H5)CH(CH3)2的名称是 ( )
A.1,3-二甲基戊烷 B.2-甲基-3-乙基丁烷
C.3,4-二甲基戊烷 D.2,3-二甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是重要的溶剂和替代燃料,工业常以CO和H2的混合气体为原料一定条件下制备甲醇。
(1)甲醇与乙醇互为 ;完全燃烧时,甲醇与同物质的量的汽油(设平均组成为C8H18)消耗O2量之比为 。
(2)工业上常用“水煤气法”获得CO和H2,其反应原理如下:
C(s) + H2O(g) ![]() CO(g) + H2(g) CO(g) + H2O(g)
CO(g) + H2(g) CO(g) + H2O(g) ![]() CO2(g) + H2(g)
CO2(g) + H2(g)
某水煤气样品中含0.2LCO、0.5LCO2,则该样品中含H2 L。
(3)工业上还可以通过下列途径获得H2,其中节能效果最好的是 。
A. 高温分解水制取H2:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
B. 电解水制取H2:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
C. 甲烷与水反应制取H2:CH4 + H2O![]() 3H2 + CO
3H2 + CO
D. 在光催化剂作用下,利用太阳能分解水制取H2:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
(4)在2L的密闭容器中充入1molCO和2molH2,一定条件下发生反应:CO(g)+2H2(g) ![]() CH3OH(g) 测得CO和CH3OH(g)浓度变化如图所示。
CH3OH(g) 测得CO和CH3OH(g)浓度变化如图所示。
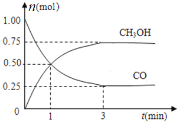
① 从反应开始到平衡,氢气的平均反应速率v(H2)= mol·(L·min)—1。
② 能够判断该反应达到平衡的是 (填选项)。
A.CO、H2和CH3OH三种物质的浓度相等
B.密闭容器中混合气体的密度不再改变
C.CH3OH分解的速率和CH3OH生成的速率相等
D.相同时间内消耗1 mol CO,同时消耗1 mol CH3OH
(5)为使合成甲醇原料的原子利用率达100%,实际生产中制备水煤气时还使用CH4,则生产投料时,n(C)∶n(H2O)∶n(CH4)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将质量为12.64g KMnO4固体加热一段时间后,收集到amolO2;向反应后残留的固体中加入足量的浓盐酸,又收集到bmolCl2,此时Mn元素全部以Mn2+的形式存在于溶液中。
(1)请完成并配平下列化学方程式:
K2MnO4+ HCl - KCl+ MnCl2+ Cl2↑+________□
该反应中的还原剂是 ,当该反应中转移NA个电子时,氧化产物的物质的量为 mol,被氧化的还原剂的物质的量为 mol。
(2)用酸性高锰酸钾溶液滴定FeSO4溶液写出该反应的离子方程式 。
(3)当KMnO4固体加热生成O2 a mol值最大时,向反应后残留的固体中加入足量的浓盐酸并加热,产生Cl2的物质的量b= mol。(此时Mn元素全部以Mn2+的形式存在于溶液中)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.海洋约占地球表面积的71%,所以地球上不缺水
B.海水淡化蒸馏法的成本最低
C.海水淡化的主要方法有蒸馏法、电渗析法和离子交换法等
D.以上说法都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置制取乙酸乙酯。回答下列问题:
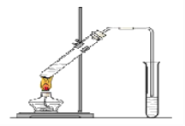
(1)写出制取乙酸乙酯的化学反应方程式: 。
(2)饱和碳酸钠溶液的主要作用是: 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是: 。
(4)应结束后,振荡试管b,静置。观察到的现象是 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是(填名称): 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶 质 | HCl | NaOH | CH3COOH | HNO3 |
溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
物质的量浓度/mol·L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是( )
A.HCl B.NaOH C.CH3COOH D.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。
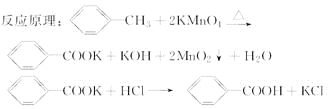
实验方法:一定量的甲苯和KMnO4溶液在100 ℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
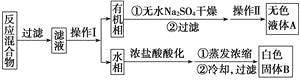
已知:苯甲酸分子量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为________,操作Ⅱ为________。
(2)无色液体A是________,定性检验A的试剂是________,现象是________。
(3)测定白色固体B的熔点,发现其在115 ℃开始熔化,达到130 ℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在完成表中内容。
序号 | 实验方案 | 实验现象 | 结果 |
① | 将白色固体B加入水中,加热溶解,________ | 得到白色晶体和无色滤液 | |
② | 取少量滤液于试管中,________ | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________ | ________ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 g产品,配成100 mL苯甲酸溶液,移取25.00 mL溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数的计算结果为________(保留2位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com