
【题目】NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下:
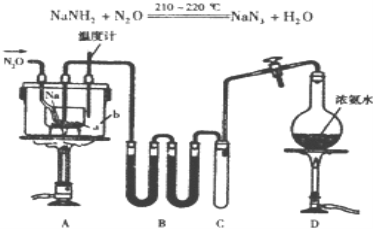
实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气.
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热D并关闭旋塞.
③向装置A中b容器内充入加热介质并加热到210一220℃,然后通入N2O.
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩、结晶.
⑤过滤,用乙醚洗涤,晾干.
已知:NaNH2熔点210℃,沸点400℃,在水溶液中易水解.
回答下列问题:
(1)图中仪器a用不锈钢材质而不用玻璃,其主要原因是___.
(2)装置B中盛放的药品为___;装置C的主要作用是___.
(3)步骤①先加热通氨气的目的是___;步骤②氨气与熔化的钠反应的方程式为___.
(4)步骤③b容器充入的介质为植物油,进行油浴而不用水浴的主要原因是___.
(5)生成NaN3的化学方程式为___.
(6)步骤⑤用乙醚洗涤的主要目的是___.
【答案】反应过程中能生成NaOH腐蚀玻璃碱石灰或固体NaOH冷凝分离出水排尽装置中的空气2Na+2NH3=2NaNH2+H2↑水的沸点为100℃,不能达到反应控制的温度210-220℃,故用油浴加热NaNH2+N2O![]() NaN3+H2O减少晶体的损失,有利于产品迅速干燥。
NaN3+H2O减少晶体的损失,有利于产品迅速干燥。
【解析】
(1)生成NaN3的化学方程式为:NaNH2+N2O![]() NaN3+H2O,反应过程中生成的水,又会与钠反应生成NaOH腐蚀玻璃,故答案为:反应过程中能生成NaOH腐蚀玻璃;
NaN3+H2O,反应过程中生成的水,又会与钠反应生成NaOH腐蚀玻璃,故答案为:反应过程中能生成NaOH腐蚀玻璃;
(2)制备的氨气中含有大量的水,用C装置盛放碱石灰干燥氨气, 用C装置冷凝分离出水,故答案为:碱石灰或固体NaOH、冷凝分离出水;
(3)步骤①先加热通氨气的目的是排尽装置中的空气。步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为:2Na+2NH3![]() 2NaNH2+H2
2NaNH2+H2![]() ,故答案为:排尽装置中的空气、2Na+2NH3=2NaNH2+H2↑;
,故答案为:排尽装置中的空气、2Na+2NH3=2NaNH2+H2↑;
(4)水的沸点为100℃,不能达到反应控制的温度210一220℃,故用油浴加热,故答案为:水的沸点为100℃,不能达到反应控制的温度210-220℃,故用油浴加热;
(5)反应物为N2O和NaNH2,生成物有NaN3,反应方程式为:NaNH2+N2O![]() NaN3+H2O;故答案为:NaNH2+N2O
NaN3+H2O;故答案为:NaNH2+N2O![]() NaN3+H2O;
NaN3+H2O;
(6)NaN3不溶于乙醚,用减少乙醚洗涤能减少晶体的损失,乙醚易挥发,有利于产品快速干燥。故答案为:减少晶体的损失,有利于产品迅速干燥。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有4瓶常用溶液:①BaCl2溶液,②NaCl溶液,③Na2SO4溶液,④CuSO4溶液。不用其他试剂,可通过实验方法将它们一一鉴别开来,鉴别出来的先后顺序是( )
A. ④③①② B. ①③④② C. ④①③② D. ①④②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化钠与过氧化钠的说法正确的是( )
A.它们属于碱性氧化物
B.它们都能与水反应产生氧气
C.它们都能与二氧化碳发生氧化还原反应
D.过氧化钠是潜水艇和呼吸面具的供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向体积为2L的密闭容器中通入NO2 (气体)和N2O4 (无色气体),二者之间可相互转化,反应过程中各物质的物质的量随时间的变化曲线如图所示。回答下列问题:

(1)0~3min内用N2O4表示的平均反应速率为___________。
(2)若升高温度,则v(正)__________(填“加快”“减慢”或“不变”,下同),v(逆)___________。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得:甲中v(NO2)=0.2mol·L-1·s-1,乙中v(N2O4)=9mol·L-1·min-1,则_________(填“甲”或“乙”)中反应更快。
(4)下列叙述能说明该反应已达到化学平衡状态的是(_____)
A v(NO2)=2 v(N2O4)
B 容器内压强不再发生变化
C X的体积分数不再发生变化
D 容器内气体的原子总数不再发生变化
E 相同时间内消耗n mol Y的同时生成2n mol X
F 相同时间内消耗n mol Y的同时消耗2n mol X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素的部分性质数据如下:
元素 | T | X | Y | Z | W |
原子半径(mm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
(1)Z离子的结构示意图为_______________。
(2)关于Y、Z两种元素,下列叙述正确的是__________(填序号)。
a 简单离子的半径Y>Z
b 气态氢化物的稳定性Y比Z强
c 最高价氧化物对应水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物。某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是____________________________。一段时间后,观察到试管中的现象是_________________________,发生反应的离子方程式是___________________________。

(4)XO2是导致光化学烟雾的“罪魁祸首”之一。它被氢氧化钠溶液吸收的化学方程式是: 2XO2+2NaOH=M+NaXO3+H2O (已配平),产物M中元素X的化合价为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是( )
A. 用湿润的pH试纸测稀碱液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D. 测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含氮化合物对能源、环保和生产具有重要的意义。请回答下列问题:
(1)在2 L密闭容器内, 800 ℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①如图所示A点处v正___(填“>”、“<”或“=”,下同)v逆,A点处v正___B点处v正。
②如图所示的曲线,其中表示NO2的变化的曲线是________(填a、b、c、d等字母)。用O2表示2 s内该反应的速率v=________。
(2)已知化学反应N2+3H2![]() 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,
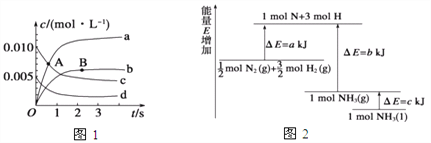
则,1 mol N和3 mol H生成1 mol NH3(g)是______能量的过程(填“吸收”或“释放”),由![]() mol N2(g)和
mol N2(g)和![]() mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。
mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题。
(1)写出下列基团(或官能团)的名称或结构简式:-OH________ 、 碳碳双键__________、
(2)相对分子质量为72且沸点最低的烷烃的结构简式_______________;
(3)对下列物质进行系统命名:
![]() :__________;CH2=CHCH2CH3:_______________;
:__________;CH2=CHCH2CH3:_______________;
(4)分子式为C4H8O2的同分异构体中,属于酯类的有______种;
(5)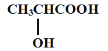 形成六元环酯的产物的结构简式__________________________。
形成六元环酯的产物的结构简式__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com