
ΓΨΧβΡΩΓΩ”–ΜζΈοAΓΔBΓΔCΓΔDΓΔEΓΔF÷°Φδ”–»γœ¬ΒΡΉΣΜ·ΙΊœΒΘΚ
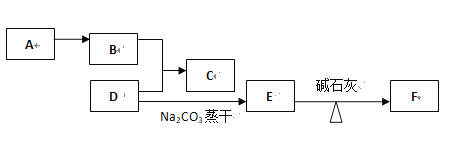
“―÷ΣF «ΫαΙΙΉνΦρΒΞΒΡΧΰΘ§C «ΨΏ”–Υ°ΙϊœψΈΕΒΡ“ΚΧεΓΔ≤Μ»ή”ΎΥ°Θ§Ζ÷Ή”÷–”–4ΗωΧΦ‘≠Ή”ΘΜA «÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΘ§ «ΚβΝΩΙζΦ“ ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΒΡ±ξ÷ΨΓΘ ‘–¥≥ωΘΚ
Θ®1Θ©FΒΡΫαΙΙ Ϋ________ Θ§Υϋ”ꬻΤχΖΔ…ζΖ¥”ΠΒΡ≤ζΈο «_________Θ®Χν¥ΩΨΜΈοΜρΜλΚœΈοΘ©
Θ®2Θ© B+DΓζCΒΡΜ·―ßΖΫ≥Χ Ϋ___________________________________;
Θ®3Θ©AΓζBΒΡΜ·―ßΖΫ≥Χ Ϋ________________Ζ¥”Πάύ–Ά_____________;
Θ®4Θ©“‘““»≤ΈΣ‘≠Νœ÷ΤΨέ¬»““œ©ΘΚ
≤Ϋ÷η“ΜΘΚΜ·―ßΖΫ≥Χ Ϋ _________________Ζ¥”Πάύ–Ά_____________;
≤Ϋ÷ηΕΰΘΚΜ·―ßΖΫ≥Χ Ϋ _________________Ζ¥”Πάύ–Ά_____________;
Θ®5Θ©ΈλΆι «FΒΡΆ§œΒΈοΘ§–¥≥ωΈλΆιΒΡΥυ”–Ά§Ζ÷“λΙΙΧε______________________________
ΓΨ¥πΑΗΓΩ ![]() ΜλΚœΈο CH3COOH + CH3CH2OH
ΜλΚœΈο CH3COOH + CH3CH2OH![]() CH3COOCH2CH3+ H2O CH2=CH2+H2O
CH3COOCH2CH3+ H2O CH2=CH2+H2O![]() CH3CH2OH Φ”≥…Ζ¥”Π CHΓ‘CH+HCl
CH3CH2OH Φ”≥…Ζ¥”Π CHΓ‘CH+HCl![]() CH2=CHCl Φ”≥…Ζ¥”Π nCH2=CHCl
CH2=CHCl Φ”≥…Ζ¥”Π nCH2=CHCl![]()
![]() Φ”ΨέΖ¥”Π CH3CH2CH2CH2CH3ΓΔCH3CH(CH3)CH2CH3ΓΔC(CH3)4
Φ”ΨέΖ¥”Π CH3CH2CH2CH2CH3ΓΔCH3CH(CH3)CH2CH3ΓΔC(CH3)4
ΓΨΫβΈωΓΩ ‘ΧβΖ÷ΈωΘΚA «÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΘ§ «ΚβΝΩΙζΦ“ ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΒΡ±ξ÷ΨΘ§A «““œ©ΘΜDΡή”κΧΦΥαΡΤΖ¥”ΠΘ§D «ΥαΘ§E «τ»ΥαΡΤΘ§F «ΫαΙΙΉνΦρΒΞΒΡΧΰΘ§F «ΦΉΆιΘ§ΡφΆΤE «““ΥαΡΤΘ§D «““ΥαΘΜC «ΨΏ”–Υ°ΙϊœψΈΕΒΡ“ΚΧεΓΔ≤Μ»ή”ΎΥ°Θ§C «θΞάύΘ§Ζ÷Ή”÷–”–4ΗωΧΦ‘≠Ή”Θ§B”κD…ζ≥…CΘ§Υυ“‘C «““Υα““θΞΘΜB «““¥ΦΘΜ
ΫβΈωΘΚΗυΨί“‘…œΖ÷ΈωΘ§Θ®1Θ©F «ΦΉΆιΘ§ΫαΙΙ ΫΈΣ![]() Θ§Υϋ”ꬻΤχΖΔ…ζ»Γ¥ζΖ¥”ΠΒΡ≤ζΈο «“Μ¬»ΦΉΆιΓΔΕ଻ֹΆιΓΔ»ΐ¬»ΦΉΆιΓΔΥΡ¬»Μ·ΧΦΒΡΜλΚœΈοΘΜΘ®2Θ©““¥Φ”κ““ΥαΖΔ…ζθΞΜ·Ζ¥”Π…ζ≥…““Υα““θΞΒΡΖΫ≥Χ Ϋ «CH3COOH + CH3CH2OH
Θ§Υϋ”ꬻΤχΖΔ…ζ»Γ¥ζΖ¥”ΠΒΡ≤ζΈο «“Μ¬»ΦΉΆιΓΔΕ଻ֹΆιΓΔ»ΐ¬»ΦΉΆιΓΔΥΡ¬»Μ·ΧΦΒΡΜλΚœΈοΘΜΘ®2Θ©““¥Φ”κ““ΥαΖΔ…ζθΞΜ·Ζ¥”Π…ζ≥…““Υα““θΞΒΡΖΫ≥Χ Ϋ «CH3COOH + CH3CH2OH![]() CH3COOCH2CH3+ H2O ;
CH3COOCH2CH3+ H2O ;
Θ®3Θ©““œ©”κΥ°ΖΔ…ζΦ”≥…Ζ¥”Π…ζ≥…““¥ΦΘ§Μ·―ßΖΫ≥Χ Ϋ «CH2=CH2+H2O![]() CH3CH2OHΘΜΘ®4Θ©“‘““»≤ΈΣ‘≠Νœ÷ΤΨέ¬»““œ©ΘΚ
CH3CH2OHΘΜΘ®4Θ©“‘““»≤ΈΣ‘≠Νœ÷ΤΨέ¬»““œ©ΘΚ
≤Ϋ÷η“ΜΘΚ““»≤”ꬻ̷«βΖΔ…ζΦ”≥…Ζ¥”Π…ζ≥…¬»““œ©Θ§Μ·―ßΖΫ≥Χ ΫCHΓ‘CH+HCl![]() CH2=CHClΘΜ≤Ϋ÷ηΕΰΘΚ¬»““œ©ΖΔ…ζΦ”ΨέΖ¥”Π…ζ≥…Ψέ¬»““œ©Θ§Μ·―ßΖΫ≥Χ Ϋ «nCH2=CHCl
CH2=CHClΘΜ≤Ϋ÷ηΕΰΘΚ¬»““œ©ΖΔ…ζΦ”ΨέΖ¥”Π…ζ≥…Ψέ¬»““œ©Θ§Μ·―ßΖΫ≥Χ Ϋ «nCH2=CHCl![]()
![]() ΘΜΘ®5Θ©ΈλΆιΒΡΥυ”–Ά§Ζ÷“λΙΙΧε”–CH3CH2CH2CH2CH3ΓΔCH3CH(CH3)CH2CH3ΓΔC(CH3)4ΓΘ
ΘΜΘ®5Θ©ΈλΆιΒΡΥυ”–Ά§Ζ÷“λΙΙΧε”–CH3CH2CH2CH2CH3ΓΔCH3CH(CH3)CH2CH3ΓΔC(CH3)4ΓΘ


 Οϊ–ΘΩΈΧΟœΒΝ–¥πΑΗ
Οϊ–ΘΩΈΧΟœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ25Γφ ±,”Ο0.100mol/LΒΡNaOH»ή“ΚΒΈΕ®20.00mL0.100mol/LΒΡHA»ή“ΚΘ§»ή“ΚΒΡPH”κΥυΦ”NaOH»ή“ΚΧεΜΐ(V)ΒΡΙΊœΒ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
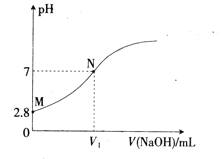
A. V1<20
B. Ka(HA)ΒΡ ΐΝΩΦΕΈΣ10-5
C. MΒψ»ή“ΚΦ”…ΌΝΩΥ°œΓ Ά,c(H+)/c(A-)‘ω¥σ
D. NΒψΚσΘ§ΥφΉ≈NaOH»ή“ΚΒΡΦ”»κ,»ή“Κ÷–Υ°ΒΡΒγάκ≥ΧΕ»÷πΫΞ‘ω¥σ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈΔ–Ά Β―ι“ρ≤ΌΉςΦρΒΞΓΔΉΑ÷Ο–Γ«…ΓΔΑ≤»ΪΩ…ΩΩΓΔΦθ…ΌΈέ»ΨΒ»ΧΊΒψΕχ±ΜΙψΖΚ”Π”ΟΘ§Εχ«“Τδ‘≠άμΚΆΙΛ“Β‘≠άμœύΆ§Θ§ΆΦ÷–Υυ Ψ « Β―ι “÷–Ϋχ––NH3ΒΡ¥ΏΜ·―θΜ· Β―ιΒΡΉΑ÷Ο(ΗΫΉ≈‘Ύ≤ΘΝßœΥΈ§…œΒΡCr2O3Ήω¥ΏΜ·ΦΝ)Θ§ΆΦ÷–ΒΡΧζΦήΧ®ΓΔΨΤΨΪΒΤΒ»“―Ψ≠¬‘»ΞΘ§»τΜ·―ß“©ΤΖΩ…Υφ±ψ»Γ”Ο(ΨΓΩ…ΡήΑ¥’’ Β―ι “÷ΤΤχΖΫΖ®≈δ÷Τ)Θ§‘ρΘΚ

Θ®1Θ©»τA÷–≤ζ…ζΒΡΤχΧε”ωΒΫHCl ΤχΧεΟΑ≥ωΑΉ―ΧΘ§≤φ–ΆΙή÷–ΒΡΙΧΧεΈο÷ A «_______Θ§ B «_______ΓΘ
(ΙΧΧεΈο÷ AΓΔBΩ…“‘ «“Μ÷÷Έο÷ “≤Ω…“‘ «Εύ÷÷Έο÷ ΒΡΜλΚœΈο)
Θ®2Θ©C¥ΠΖΔ…ζ Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ______________Θ§ΗΟΖ¥”Π÷–ΜΙ‘≠ΦΝ «_______ΘΜ‘ΎΙΛ“Β …œΘ§ΗΟΖ¥”Π“Σ«σΤχΧε_______(ΤχΧεΟϊ≥Τ) ΙΐΝΩΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΔΌFe‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ[Ar]_________,Mg‘≠Ή”ΚΥΆβ’ΦΨίΉνΗΏΡή≤ψΒγΉ”ΒΡΒγΉ”‘Τ¬÷άΣΆΦ–ΈΉ¥ΈΣ_________ΓΘ
ΔΎAsΒΡ¬±Μ·ΈοΒΡ»έΒψ»γœ¬ΘΚ
AsCl3 | AsBr3 | AsI3 | |
»έΒψ/K | 256.8 | 304 | 413 |
±μ÷–¬±Μ·Έο»έΒψ≤ν“λΒΡ‘≠“ρ «_________,AsCl3Ζ÷Ή”ΒΡΝΔΧεΙΙ–ΆΈΣ_________ΓΘ
(2)Έ§…ζΥΊB1Ω…ΉςΈΣΗ®ΟΗ≤Έ”κΧ«ΒΡ¥ζ–ΜΘ§≤Δ”–±ΘΜΛ…ώΨ≠œΒΆ≥ΒΡΉς”ΟΓΘΗΟΈο÷ ΒΡΫαΙΙ ΫΈΣ

“‘œ¬ΙΊ”ΎΈ§…ζΥΊB1ΒΡΥΒΖ®’ΐ»ΖΒΡ «________ΓΘ
AΘ°÷ΜΚ§Π“ΦϋΚΆΠ–Φϋ
BΘ°Φ»”–Ι≤ΦέΦϋ”÷”–άκΉ”Φϋ
CΘ°ΗΟΈο÷ ΒΡ»έΒψΩ…ΡήΗΏ”ΎNaCl
DΘ°ΗΟΈο÷ “Ή»ή”Ύ―ΈΥα
(3)Έ§…ζΥΊB1ΨßΧε»ή”ΎΥ°ΒΡΙΐ≥Χ÷–“ΣΩΥΖΰΒΡΈΔΝΘΦδΉς”ΟΝΠ”–________ΓΘ
AΘ°άκΉ”ΦϋΓΔΙ≤ΦέΦϋ BΘ°άκΉ”ΦϋΓΔ«βΦϋΓΔΙ≤ΦέΦϋ
CΘ°«βΦϋΓΔΖΕΒ¬ΜΣΝΠ DΘ°άκΉ”ΦϋΓΔ«βΦϋΓΔΖΕΒ¬ΜΣΝΠ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈΣΧΫΨΩΧζΚΆΧζΒΡΜ·ΚœΈοΒΡ“Μ–©Μ·―ß–‘÷ Θ§Ρ≥―ß…ζ Β―ι–ΓΉι…ηΦΤΝΥ“‘œ¬ Β―ιΓΘ
Θ®1Θ©ΆυAΓΔB»ή“Κ÷–Ζ÷±πΒΈ»κΦΗΒΈKSCN»ή“ΚΘ§»ή“ΚΒΡ―’…ΪA________Θ§B____________ΓΘ
Θ®2Θ©–¥≥ω…œ ωΙΐ≥Χ÷–”–ΙΊΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
Fe2O3ΓζA_______________________ΘΜAΓζB____________________________ΓΘ
Θ®3Θ©BΓζCΩ…Ω¥ΒΫΒΡœ÷œσ «___________________________________________ΓΘ
Θ®4Θ©ΫΪAΒΡ±ΞΚΆ»ή“ΚΒΈ»κΖ–Υ°÷–≤Δ≤ΜΕœΦ”»»Θ§Ω…÷ΤΒΟ_______________ΫΚΧεΘΜΒ±Ιβ χΆ®ΙΐΗΟΫΚΧε ±Θ§Ω…Ω¥ΒΫ“ΜΧθΙβΝΝΒΡΓΑΆ®¬ΖΓ±Θ§’β÷÷œ÷œσ≥ΤΈΣ___________–ß”ΠΓΘ
ΓΨ¥πΑΗΓΩ―ΣΚλ…Ϊ ≤Μ±δΘ®«≥¬Χ…ΪΘ© Fe2O3+6HCl=2FeCl3+3H2O Fe+2FeCl3=3FeCl2 ΑΉ…Ϊ≥ΝΒμΉΣ±δΈΣΜ“¬Χ…Ϊ”÷ΉΣ±δΈΣΚλΚ÷…Ϊ Fe(OH)3 ΕΓ¥οΕϊ
ΓΨΫβΈωΓΩ
Θ®1Θ©―θΜ·Χζ”κ―ΈΥαΖ¥”Π…ζ≥…¬»Μ·ΧζΘ§¬»Μ·Χζ”κΧζΖ¥”Π…ζ≥…¬»Μ·―«ΧζΘ§“ρ¥ΥΆυAΓΔB»ή“Κ÷–Ζ÷±πΒΈ»κΦΗΒΈKSCN»ή“ΚΘ§»ή“ΚA÷–œ‘―ΣΚλ…ΪΘ§B÷–≤Μ±δ…ΪΘΜΘ®2Θ©Fe2O3”κ―ΈΥαΖ¥”ΠΒΡΖΫ≥Χ ΫΈΣFe2O3+6HCl=2FeCl3+3H2OΘ§AΓζBΒΡΖΫ≥Χ ΫΈΣFe+2FeCl3=3FeCl2ΓΘΘ®3Θ©¬»Μ·―«Χζ”κ«β―θΜ·ΡΤΖ¥”Π…ζ≥…«β―θΜ·―«ΧζΘ§«β―θΜ·―«Χζ≤ΜΈ»Ε®Θ§“Ή±Μ―θΜ·Θ§Υυ“‘BΓζCΩ…Ω¥ΒΫΒΡœ÷œσ «ΑΉ…Ϊ≥ΝΒμΉΣ±δΈΣΜ“¬Χ…Ϊ”÷ΉΣ±δΈΣΚλΚ÷…ΪΓΘΘ®4Θ©ΫΪ¬»Μ·Χζ±ΞΚΆ»ή“ΚΒΈ»κΖ–Υ°÷–≤Δ≤ΜΕœΦ”»»Θ§Ω…÷ΤΒΟ«β―θΜ·ΧζΫΚΧεΘΜΒ±Ιβ χΆ®ΙΐΗΟΫΚΧε ±Θ§Ω…Ω¥ΒΫ“ΜΧθΙβΝΝΒΡΓΑΆ®¬ΖΓ±Θ§’β÷÷œ÷œσ≥ΤΈΣΕΓ¥οΕϊ–ß”ΠΓΘ
ΓΨΧβ–ΆΓΩ Β―ιΧβ
ΓΨΫα χΓΩ
28
ΓΨΧβΡΩΓΩœ÷”–Ρ≥ΧζΧΦΚœΫπΘ§Ρ≥Μ·―ß–Υ»Λ–ΓΉιΈΣΝΥ≤βΕ®ΧζΧΦΚœΫπ÷–ΧζΒΡ÷ ΝΩΖ÷ ΐΘ§≤ΔΧΫΨΩ≈®ΝρΥαΒΡΡ≥–©–‘÷ Θ§…ηΦΤΝΥœ¬ΆΦΥυ ΨΒΡ Β―ιΉΑ÷ΟΚΆ Β―ιΖΫΑΗΘ®Φ–≥÷“«Τς“― Γ¬‘Θ©Θ§«κΡψ≤Έ”κ¥ΥœνΜνΕ·≤ΔΜΊ¥πœύ”ΠΈ Χβ(”… Β―ιΉΑ÷Ο“ΐΤπΒΡ Β―ιΈσ≤νΚω¬‘≤ΜΦΤ)ΓΘ

IΓΔΧΫΨΩ≈®ΝρΥαΒΡΡ≥–©–‘÷
Θ®1Θ©Α¥ΆΦ ΨΝ§Ϋ”ΉΑ÷ΟΘ§Φλ≤ιΉΑ÷Ο___________Θ§≥ΤΝΩEΒΡ÷ ΝΩΓΘ
Θ®2Θ©ΫΪa®άΧζΧΦΚœΫπ―υΤΖΖ≈»κA÷–Θ§‘ΌΦ”»κ ΝΩΒΡ≈®ΝρΥαΘ§“«ΤςAΒΡΟϊ≥ΤΈΣ______Θ§Έ¥Βψ»ΦΨΤΨΪΒΤ«ΑΘ§AΓΔB ΨυΈόΟςœ‘œ÷œσΘ§Τδ‘≠“ρ «______________________ΓΘ
Θ®3Θ©Βψ»ΦΨΤΨΪΒΤ“ΜΕΈ ±ΦδΚσΘ§AΓΔB÷–Ω…Ιέ≤λΒΫΟςœ‘ΒΡœ÷œσΘ§»γA÷–![]() Θ§–¥≥ωA÷–CΚΆ≈®ΝρΥαΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ__________________________Θ§B÷–ΒΡœ÷œσ «_________________Θ§“ρ¥ΥΩ…ΒΟΒΫ≈®ΝρΥαΨΏ”–_____________–‘ΓΘ
Θ§–¥≥ωA÷–CΚΆ≈®ΝρΥαΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ__________________________Θ§B÷–ΒΡœ÷œσ «_________________Θ§“ρ¥ΥΩ…ΒΟΒΫ≈®ΝρΥαΨΏ”–_____________–‘ΓΘ
Θ®4Θ©ΥφΉ≈Ζ¥”ΠΒΡΫχ––Θ§≈®ΝρΥα≈®Ε»÷πΫΞΦθ–Γ±δΈΣœΓΝρΥαΘ§A÷–ΜΙΩ…ΡήΖΔ…ζΡ≥–©άκΉ”Ζ¥”ΠΘ§–¥≥ωœύ”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ_________________ΓΔ____________________ΓΘ
IIΓΔ≤βΕ®ΧζΒΡ÷ ΝΩΖ÷ ΐ
Θ®5Θ©¥ΐA÷–ΙΧΧεΆξ»Ϊœϊ ß≤Δ≤Μ‘Ό“ί≥ωΤχΧε ±Θ§ΆΘ÷ΙΦ”»»Θ§≤πœ¬E≤Δ≥Τ÷ΊΘ§E‘ω÷ΊbgΓΘΧζΧΦΚœΫπ÷–ΧζΒΡ÷ ΝΩΖ÷ ΐΈΣ___________________(–¥±μ¥ο Ϋ)ΓΘ
Θ®6Θ©Ρ≥Ά§―ß»œΈΣ…œ ωΖΫΖ®ΫœΗ¥‘”Θ§ Ι”Ο»γΆΦΥυ ΨΒΡΉΑ÷ΟΚΆΤδΥϊ≥Θ”ΟΒΡ Β―ι“«Τς≤βΕ®Ρ≥–© ΐΨίΦ¥Ω…ΓΘΈΣΝΥΩλΥΌΚΆΉΦ»ΖΒΊΦΤΥψ≥ωΧζΒΡ÷ ΝΩΖ÷ ΐΘ§ΉνΦρ±ψΒΡ Β―ι≤ΌΉς «___________Θ®Χν–¥¥ζΚ≈Θ©ΓΘ

ΔΌ”Ο≈≈Υ°Ζ®≤βΕ®H2ΒΡΧεΜΐ
ΔΎΖ¥”ΠΫα χΚσΘ§Ιΐ¬ΥΓΔœ¥Β”ΓΔΗ…‘οΓΔ≥ΤΝΩ≤–‘ϋΒΡ÷ ΝΩ
Δέ ≤βΕ®Ζ¥”Π«ΑΚσΉΑ÷ΟΚΆ“©ΤΖΒΡΉή÷ ΝΩag
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ « (ΓΓ )
A. ΝρΥαΓΔ¥ΩΦνΓΔ¥ΉΥαΡΤΚΆ…ζ ·Μ“Ζ÷±π τ”ΎΥαΓΔΦνΓΔ―ΈΚΆ―θΜ·Έο
B. ’αΧ«ΓΔΝρΥαΡΤΚΆΥ°Ζ÷±π τ”ΎΖ«ΒγΫβ÷ ΓΔ«ΩΒγΫβ÷ ΚΆ»θΒγΫβ÷
C. Βψ»ΦΒΡΟΨΧθ≤ΜΡή‘ΎΕΰ―θΜ·ΧΦΤχΧε÷–ΦΧ–χ»Φ…’
D. Κ§0.2molH2SO4ΒΡ≈®ΝρΥα”κΉψΝΩΒΡΆ≠Ζ¥”Π,…ζ≥…±ξΉΦΉ¥Ωωœ¬ΒΡΤχΧε2.24L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ…ηNAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A. ±ξΉΦΉ¥Ωωœ¬Θ§11.2 LCH2Cl2÷–Κ§”–Ζ÷Ή”ΒΡ ΐΡΩΈΣ0.5NA
B. ≥ΘΈ¬œ¬a gΡ≥ΆιΧΰΘ®CnH2n+2Θ©÷–Κ§”–Ι≤”ΟΒγΉ”Ε‘ ΐΡΩΈΣ![]() Θ®3n+1Θ©NA
Θ®3n+1Θ©NA
C. 56 g Ψέ““œ©÷–Κ§”–ΧΦΧΦΥΪΦϋΒΡ ΐΡΩΈΣ2NA
D. ≥ΘΈ¬œ¬Θ§0.2 mol/LΒΡFeCl3»ή“Κ÷–Κ§Cl©¹ ΐΡΩΈΣ0.6NA
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–”–ΙΊΆ§Ζ÷“λΙΙΧε ΐΡΩΒΡ–π ω¥μΈσΒΡ «Θ® Θ©
A. ΦΉ±Ϋ±ΫΜΖ…œΒΡ“ΜΗω«β‘≠Ή”±ΜΚ§3ΗωΧΦ‘≠Ή”ΒΡΆιΜυ»Γ¥ζΘ§ΥυΒΟ≤ζΈοΉνΕύ”–6÷÷
B. ΝΣ±Ϋ(![]() )ΒΡ“Μ¬»¥ζΈο”–3÷÷Θ§Ε଻¥ζΈο”–12÷÷
)ΒΡ“Μ¬»¥ζΈο”–3÷÷Θ§Ε଻¥ζΈο”–12÷÷
C. ±ϊΆιΒΡ“Μ¬»¥ζΈο”–2 ÷÷Θ§±ϊΆιΒΡΕ଻¥ζΈο”–4 ÷÷
D. Ζ÷Ή” ΫΈΣC7H8OΘ§«“ τ”ΎΖΦœψΉεΜ·ΚœΈοΒΡΆ§Ζ÷“λΙΙΧε÷Μ”–4 ÷÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩTΓφœ¬Θ§»ΐ÷÷ΝρΥα―ΈMSO4 (M: Pb2+ΓΔBa2+ΓΔSr2+)ΒΡ≥ΝΒμ»ήΫβΤΫΚβ«ζœΏ»γΆΦΥυ ΨΓΘ“―÷ΣpM=-lgc(M)Θ§p(SO42-)=-lgc(SO42-)ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
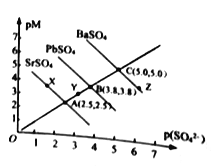
A. »ήΕ»Μΐ:BaSO4>PbSO4>SrSO4
B. Y ΒψΕ‘SrSO4 «≤Μ±ΞΚΆ»ή“ΚΘ§ΡήΦΧ–χ»ήΫβSrSO4
C. ZΒψΕ‘”ΠΒΡ»ή“Κ÷–c(Ba2+)42-)Θ§Εΰ’ΏΒΡ≈®Ε»ΜΐΒ»”Ύ1ΓΝ10-10
D. BaSO4≤Μ Ω…ΡήΉΣΜ·≥…PbSO4
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com