
下列描述正确的个数是( )
① 聚乳酸的结构为 ,聚乳酸是由单体之间通过加聚而合成
,聚乳酸是由单体之间通过加聚而合成
②完全燃烧 等物质的量的乙醛和乙醇,消耗氧气的质量相等
等物质的量的乙醛和乙醇,消耗氧气的质量相等
③蔗糖.麦芽糖的分子式都是C12H22O11,二者互为同分异构体
④用甘氨酸(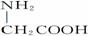 )和丙氨酸(
)和丙氨酸( )缩合最多可形成4种二肽
)缩合最多可形成4种二肽
⑤
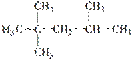 的系统命名法的名称为2,2,3-三甲基戊烷
的系统命名法的名称为2,2,3-三甲基戊烷
A. 1 B.2 C.3 D.4
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法正确的是
A.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增多
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
把6molA和5molB两气体通入容积为4L的密闭容器中,一定条件下反应:
3A(g)+B(g)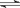 2C(g)+x D(g)△H > 0,5min达平衡,此时生成2molC,测得D的
2C(g)+x D(g)△H > 0,5min达平衡,此时生成2molC,测得D的
平均反应速率为0.1mol·(L·min)-1。下列说法中正确的是( )
A.降低平衡体系的温度,逆反应速率减小,正反应速率增大,平衡正向移动
B.恒温下达到平衡的标志是C和D的生成速率相等
C.A的平均反应速率为0.15mol·(L·min)-1
D.B的转化率为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.标准状况下,22.4 L二氯甲烷的分子数约为NA个
B.盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol
C.17.6 g丙烷中所含的极性共价键为4NA个
D.电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量一定减少64 g
查看答案和解析>>
科目:高中化学 来源: 题型:
苯甲酸广泛用于医药、食品、染料、化工等领域。以下是实验室制备苯甲酸的一种方法。反应原理如下:

 实验步骤:
实验步骤:
下图组装反应装置(冷凝水.夹持及加热装置未画出),并在三颈烧瓶中依次加入120mL水、9.4g高锰酸钾和3.0mL甲苯。
②将三颈烧瓶中的混合液体搅拌,加热至沸腾,直到甲苯完全反应。
③趁热过滤反应混合物。若滤液呈紫色,则需加入适量的亚硫酸氢钠溶液至紫色褪去后再过滤,用热水洗涤滤渣,洗涤液合并至滤液中。
④用冰水冷却滤液,然后用浓盐酸酸化,过滤,用少量冷水洗涤滤渣,得到苯甲酸粗产品,经重结晶得到精制的苯甲酸。
回答下列问题:
(1)本实验应选择的三颈烧瓶规格为 (填字母序号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)判断甲苯已完全反应的现象是 、回流液不再出现油珠。
(3)实验步骤④中,用少量冷水而不用热水洗涤滤渣的目的是 ;
苯甲酸粗产品除了可用重结晶法精制外,还可用 法。
A.蒸发 B.升华 C.过滤 D.分液
(4)精制的苯甲酸纯度测定:称取1.220g样品,用稀乙醇溶解并配成100 mL溶液,分别取25.00mL溶液,用0.1000 mo1·L-1NaOH标准溶液滴定,三次滴定消耗NaOH溶液的体积分别为V1=24.70mL、V2=24.80 mL、V3= 25.80mL。
①配制溶液时用稀乙醇而不 用蒸馏水作溶剂的原因是 。
用蒸馏水作溶剂的原因是 。
②若用酚酞作指示剂,确定滴定终点 的现象是 。
的现象是 。
③产品的纯度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学实验装置的正确连接是实验成功的关键,下图是中学化学中常见的实验装置。
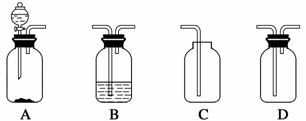
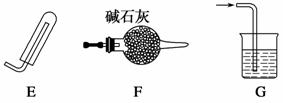
(1)用上述装置制备气体:
①若B中盛放浓硫酸,则A、B、C组合后能制取并收集的气体是________。
a.H2 b.H2S
c.CO2 d.C2H2
②要快速制取并得到干燥的NH3,正确的仪器组合是____(按制气装置顺序填仪器的编号字母),制气所选用的固体药品是__________。
③若用H2O2和MnO2来制取和收集干燥的O2,则应选择的仪器正确组合是__________(按制气装置顺序填仪器的编号字母),检验气体收集满的方法是________________。
(2)甲同学用A、B组合来验证盐酸、碳酸、次氯酸的酸性强弱时,盐酸应装入__________(填仪器名称)中,B装置中发生反应的离子方程式为_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中通入一定量SO2后,不会出现沉淀的是( )
A.Na2S溶液 B.BaCl2溶液
C.Ba(NO3)2溶液 D.NaClO和BaCl2混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要90 mL浓度为1 mol·L-1的稀硫酸,现用18.4 mol·L-1的浓硫酸配制,其操作可分为以下各步:
A.用量筒量取5.4mL浓硫酸缓缓注入装有约10 mL蒸馏水的烧杯中,并用玻璃棒不断搅拌后,静置____________;
B.用约20 mL蒸馏水,分三次洗涤烧杯和玻璃棒,将每次洗液都倒入容量瓶里;
C.将稀释后稀硫酸小心倒入____________mL容量瓶里;
D.检查所选容量瓶是否会发生漏液;
E.将蒸馏水直接加入容量瓶,至液面距离刻度线________________处;
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液;
G.用胶头滴管向容量瓶里逐滴滴入蒸馏水,目光平视,滴至_____________。
(1)填写上述各步的空白处。
(2)正确的操作顺序是D A C _____________ F (填写字母)。
(3)进行A步操作应选择下列量器:①10 mL量筒;②50 mL量筒;500 mL量筒;④1 000 mL量筒中的______(填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com