
| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
分析 (1)水解是吸热过程,升温HCO3-的水解程度增大,故碱性增强,碳酸氢根离子水解生成碳酸和氢氧根离子;
(2)碳酸钠是强碱弱酸盐能水解,且碳酸钠的水解程度大于碳酸氢钠的水解程度;
(3)依据冷却到室温溶液PH中的分析反应过程中生成了新的物质;碳酸钠水解程度大于碳酸氢钠,溶液减小增强.
解答 解:(1)碳酸氢钠是强碱弱酸酸式盐,能水解导致溶液呈碱性,升高温度,HCO3-的水解程度增大,故碱性增强,水解方程式为:HCO3-+H2O?H2CO3+OH-;
故答案为:HCO3-+H2O?H2CO3+OH-;
(2)碳酸钠是强碱弱酸盐能水解,碳酸是二元弱酸,第一步电离程度远远大于第二步电离,所以碳酸根离子的第一步水解程度远远大于第二步水解程度,导致碳酸钠的水解程度大于碳酸氢钠的水解程度,
故答案为:大于;
(3)将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1,溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成;所以乙正确;
故答案为:乙;溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成.
点评 本题碳酸氢钠考查了碳酸氢钠的性质,实验探究物质性质的设计方案,反应产物的判断,盐类水解的分析应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | c(Na+)=c(NH2-) | B. | c(NH4+)=1×10-29 mol•L-1 | ||
| C. | c(NH2-)>c(NH4+) | D. | c(NH4+).c(NH2-)=1.0×10-30 mol2•L-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
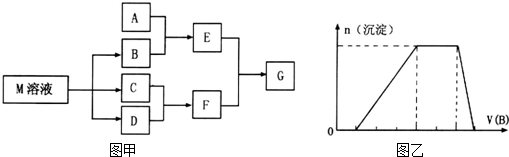
 (3)装置B中试剂的作用是检验SO2是否除尽.
(3)装置B中试剂的作用是检验SO2是否除尽.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
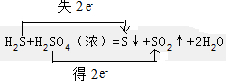 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-、Cl- | B. | Na+、Cu2+ | C. | Mg2+、C1- | D. | C1-、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硫元素既被氧化又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 当转移8mol电子时,还原产物比氧化产物多1mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com