
| A、氯化氢溶于水 |
| B、加热氯酸钾使其分解 |
| C、碘升华 |
| D、氯化钠溶于水 |
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
A、 即使MnO2过量,盐酸也不能全部消耗 |
B、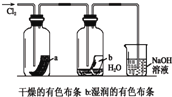 湿润的有色布条能褪色 |
C、 生成棕色的烟 |
D、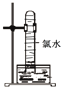 用光照射氯水后液体颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO32-+H2O?HCO3-+OH 用热的纯碱溶液清洗油污 |
| B、Al3++3H2O?Al(OH)3+H+ 明矾净水 |
| C、TiCl4+(x+2)H2O(过量)?TiO2?x H2O↓+4HCl 用TiCl4制备TiO2 |
| D、SnCl2+H2O?Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸铵自发地溶于水 |
| B、2N2O5(g)=4NO2 (g)+O2(g)△H=+156.7kJ/mol |
| C、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)△H=+74.9 kJ/mol |
| D、2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有②④⑤ |
| B、只有②③⑥ |
| C、只有①③⑤ |
| D、只有④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过渡元素形成的化合物 |
| B、第IIIA族元素形成的化合物 |
| C、第VIIA族元素形成的化合物 |
| D、第IVA族元素形成的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:


| 乙装置的质量/g | 丙装置的质量/g | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com