
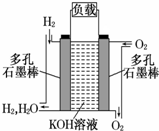
 ±»ÓžĪŖøıäĪ“Ą“ŹĄ½ēµÄŹ®“óŠĀæĘ¼¼Ö®Ņ»µÄČ¼ĮĻµē³Ų¾ßÓŠĪŽĪŪČ¾”¢ĪŽŌėŅō”¢øߊ§ ĀŹµÄĢŲµć£®ČēĶ¼ĪŖĒāŃõČ¼ĮĻµē³ŲµÄ½į¹¹Ź¾ŅāĶ¼£¬µē½āÖŹČÜŅŗĪŖKOH ČÜŅŗ£¬µē¼«²ÄĮĻĪŖŹčĖɶąæ׏ÆÄ«°ō£®µ±ŃõĘųŗĶĒāĘų·Ö±šĮ¬ Šų²»¶ĻµŲ“ÓÕż”¢øŗĮ½¼«ĶØČėČ¼ĮĻµē³ŲŹ±£¬±ćæÉŌŚ±ÕŗĻ»ŲĀ·ÖŠ²»¶ĻµŲ²śÉśµēĮ÷£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
±»ÓžĪŖøıäĪ“Ą“ŹĄ½ēµÄŹ®“óŠĀæĘ¼¼Ö®Ņ»µÄČ¼ĮĻµē³Ų¾ßÓŠĪŽĪŪČ¾”¢ĪŽŌėŅō”¢øߊ§ ĀŹµÄĢŲµć£®ČēĶ¼ĪŖĒāŃõČ¼ĮĻµē³ŲµÄ½į¹¹Ź¾ŅāĶ¼£¬µē½āÖŹČÜŅŗĪŖKOH ČÜŅŗ£¬µē¼«²ÄĮĻĪŖŹčĖɶąæ׏ÆÄ«°ō£®µ±ŃõĘųŗĶĒāĘų·Ö±šĮ¬ Šų²»¶ĻµŲ“ÓÕż”¢øŗĮ½¼«ĶØČėČ¼ĮĻµē³ŲŹ±£¬±ćæÉŌŚ±ÕŗĻ»ŲĀ·ÖŠ²»¶ĻµŲ²śÉśµēĮ÷£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ £®
£® ·ÖĪö £Ø1£©ĒāŃõČ¼ĮĻµē³ŲÖŠ£¬µē½āÖŹČÜŅŗĪŖ¼ī£¬Ōņøŗ¼«ÉĻĒāĘųµĆµē×ÓÉś³ÉĖ®£»
£Ø2£©±ūĶéŗĶ H2O·“Ӧɜ³É H2 ŗĶ CO£¬½įŗĻÖŹĮæŹŲŗćŹéŠ“·½³ĢŹ½£»
£Ø3£©Č¼ĮĻµē³ŲÖŠ£¬øŗ¼«ÉĻČ¼ĮĻŹ§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£»¼īŠŌĢõ¼žĻĀ£¬¼×ĶéČ¼ÉÕÉś³ÉĢ¼ĖįøłĄė×Ó£»
£Ø4£©øł¾Żn=$\frac{m}{M}$¼ĘĖćÓŠ»śĪļA”¢¶žŃõ»ÆĢ¼”¢Ė®µÄĪļÖŹµÄĮ棬øł¾ŻŌ×ÓŹŲŗć¼ĘĖćĢž·Ö×ÓÖŠC”¢HŌ×ÓŹżÄ棬øł¾ŻĻą¶ŌŌ×ÓÖŹĮæ¼ĘĖć·Ö×ÓÖŠŃõŌ×ÓŹżÄ棬¾Ż“ĖŹéŠ“øĆĢžµÄ·Ö×ÓŹ½£»ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶĪ»ÓŚ·Ö×Ó¶ĖµÄC”ŌC¼ü£¬ŗĖ“Ź²ÕńĒāĘ×ÓŠČżøö·å£¬·åĆ껿ĪŖ6£ŗ1£ŗ1£¬·Ö×ÓÖŠÓŠ3ÖÖ²»Ķ¬µÄHŌ×Ó£¬Ō×ÓŹżÄæÖ®±ČĪŖ6£ŗ1£ŗ1£¬½įŗĻÓŠ»śĪļµÄ·Ö×ÓŹ½ÅŠ¶ĻÓŠ»śĪļAµÄ½į¹¹£®
½ā“š ½ā£ŗ£Ø1£©ĒāŃõČ¼ĮĻµē³ŲÖŠ£¬µē½āÖŹČÜŅŗĪŖ¼ī£¬Ōņøŗ¼«ÉĻĒāĘųµĆµē×ÓÉś³ÉĖ®£¬ŌņĘäµē¼«·“Ó¦Ź½ĪŖ£ŗ2H2+4OH--4e-ØT4H2O£¬¹Ź“š°øĪŖ£ŗ2H2+4OH--4e-ØT4H2O£»
£Ø2£©±ūĶéŗĶ H2O·“Ӧɜ³É H2 ŗĶ CO£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖC3H8+3H2O$\frac{\underline{“߻ƼĮ}}{”÷}$3CO+7H2£¬¹Ź“š°øĪŖ£ŗC3H8+3H2O$\frac{\underline{“߻ƼĮ}}{”÷}$3CO+7H2£»
£Ø3£©Č¼ĮĻµē³ŲÖŠ£¬øŗ¼«ÉĻČ¼ĮĻŹ§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬¼īŠŌĢõ¼žĻĀ£¬¼×ĶéŌŚøŗ¼«Éś³ÉĢ¼ĖįøłĄė×Ó£¬Ęäµē¼«·“Ó¦Ź½ĪŖ£ŗCH4+10OH--8e-ØTCO32-+7H2O£»¼īŠŌĢõ¼žĻĀ£¬¼×ĶéČ¼ÉÕÉś³ÉµÄ¶žŃõ»ÆĢ¼ŌŁÓėĒāŃõøłĄė×Ó½įŗĻÉś³ÉĢ¼ĖįøłĄė×Ó£¬Ōņ×Ü·“Ó¦·½³ĢŹ½ĪŖCH4+2O2+2OH-ØTCO32-+3H2O£¬
¹Ź“š°øĪŖ£ŗCH4+10OH--8e-ØTCO32-+7H2O£»CH4+2O2+2OH-ØTCO32-+3H2O£»
£Ø4£©ÓŠ»śĪļAÖ»ŗ¬ÓŠC”¢H”¢OČżÖÖŌŖĖŲ£¬ÖŹĘ×Ķ¼±ķĆ÷ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ84£¬16.8gÓŠ»śĪļAµÄĪļÖŹµÄĮæĪŖ0.2mol£¬¾Č¼ÉÕÉś³É44.0g CO2£¬ĪļÖŹµÄĮæĪŖ1mol£¬Éś³É14.4g H2O£¬ĪļÖŹµÄĮæĪŖ$\frac{14.4g}{18g/mol}$=0.8mol£¬¹ŹÓŠ»śĪļAÖŠCŌ×ÓŹżÄæĪŖ$\frac{1mol}{0.2mol}$=5£¬HŌ×ÓŹżÄæĪŖ$\frac{0.8mol”Į2}{0.2mol}$=8£¬¹ŹŃõŌ×ÓŹżÄæĪŖ$\frac{84-12”Į5-8}{16}$=1£¬¹ŹAµÄ·Ö×ÓŹ½ĪŖC5H8O£¬
²»±„ŗĶ¶ČĪŖ$\frac{2”Į5+2-8}{2}$=2£¬ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶĪ»ÓŚ·Ö×Ó¶ĖµÄC”ŌC¼ü£¬ŗĖ“Ź²ÕńĒāĘ×ÓŠČżøö·å£¬·åĆ껿ĪŖ6£ŗ1£ŗ1£¬¹Ź·Ö×ÓÖŠŗ¬ÓŠ2øöCH3”¢1øö-OHĮ¬½ÓŌŚĶ¬Ņ»CŌ×ÓÉĻ£¬¹ŹAµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗC5H8O£» £®
£®
µćĘĄ ±¾Ģāæ¼²éČ¼ĮĻµē³Ų¼°ĪļÖŹµÄĮæµÄÓŠ¹Ų¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦µÄ漲飬עŅā°ŃĪÕŌµē³ŲµÄ¹¤×÷ŌĄķŅŌ¼°øł¾Żµē¼«·½³ĢŹ½ÖŠµē×ÓÓėĪļÖŹµÄ¹ŲĻµĒóĖć£¬ĢāÄæÄѶČÖŠµČ£®


 æĪĢĆĮ·¼Ó²āĻµĮŠ“š°ø
æĪĢĆĮ·¼Ó²āĻµĮŠ“š°ø ĒįĖÉæĪĢƵ„ŌŖ²āŹŌAB¾ķĻµĮŠ“š°ø
ĒįĖÉæĪĢƵ„ŌŖ²āŹŌAB¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĪĀ¶Č/”ę | 25 | 80 | 230 |
| Ę½ŗā³£Źż | 5”Į104 | 2 | 1.9”Į10-5 |
| A£® | ÉĻŹöÉś³ÉNi£ØCO£©4µÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦ | |
| B£® | ŌŚ80”ꏱ£¬²āµĆijŹ±æĢNi£ØCO£©4”¢COµÄÅØ¶Č¾łĪŖ0.5 mol•L-1£¬Ōņ“ĖŹ±vÕż£¾vÄę | |
| C£® | 25”ꏱ·“Ó¦Ni£ØCO£©4£Øg£© Ni£Øs£©+4CO£Øg£©µÄĘ½ŗā³£ŹżĪŖ2”Į10-5 | |
| D£® | 80”ę“ļµ½Ę½ŗāŹ±£¬²āµĆn£ØCO£©=0.3 mol£¬ŌņNi£ØCO£©4µÄĘ½ŗāÅضČĪŖ2 mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõČ¼ĮĻµē³ŲŹĒŅ»ÖÖ½«»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵÄ×°ÖĆ | |
| B£® | Ģś“¬²°µÄĶāæĒÉĻĻāĒ¶Šææ飬æɱÜĆā“¬ĢåŌāŹÜøÆŹ“ | |
| C£® | øÖĢśøÆŹ“Ź±øŗ¼«µÄµē¼«·“Ó¦Ź½£ŗFe-3e-ØTFe+ | |
| D£® | ¹¤ŅµÉĻµē½ā±„ŗĶŹ³ŃĪĖ®Ź±Ņõ¼«µÄµē¼«·“Ó¦Ź½£ŗ2H++2e-ØTH2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C2H4O2 | B£® | C3H8O | C£® | C3H7Cl | D£® | C5H12 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | OH- | B£® | Ag+ | C£® | Na+ | D£® | Ba2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4øö | B£® | 5øö | C£® | 6øö | D£® | 7øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČČ»Æѧ·½³ĢŹ½ÖŠ£¬»ÆѧŹ½Ē°ĆęµÄ»Æѧ¼ĘĮæŹżÖ»ÄܱķŹ¾ĪļÖŹµÄĮæ | |
| B£® | 1 moL H2Éś³É1 mol H20Ź±·Å³öµÄČČĮæ¾ĶŹĒĒāĘųµÄČ¼ÉÕČȵÄÖµ | |
| C£® | ÓĆ1mol/LµÄĮņĖįŗĶŹŹĮæµÄĻ”µÄBa£ØOH£©2ČÜŅŗ·“Ó¦æÉŅŌ²āĮæÖŠŗĶČȵÄÖµ | |
| D£® | Ģõ¼žĻąĶ¬£¬ÓĆ16g¹ĢĢåĮņ»ņ32 g¹ĢĢåĮņ·Ö±šŌŚ02ÖŠ³ä·ÖČ¼ÉÕ£¬²ā¶ØµÄĮņµÄČ¼ÉÕČČ²»Ķ¬ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com