
| A. | ①②⑤ | B. | ①② | C. | ①②③ | D. | ①②③⑤ |
分析 游离态是元素以单质的形式存在,化合态是元素在化合物中的形式存在,元素在自然界中的存在状态与元素的活泼性有密切的关系,活泼元素在自然界中以化合物的形式存在,不活泼的元素在自然界中以单质的形式存在.
解答 解:①硅元素自然界中以硅酸盐或二氧化硅形式,不存在游离态的硅,故正确;
②Al为比较活泼的金属,易被氧化,从而性质活泼,在自然界中只能以化合物的形式存在,故正确;
③Cl最外层电子为7,易得到,易被还原,从而性质活泼,在自然界中只能以化合物的形式存在,故正确;
④Fe在自然界中以化合态,只有少量陨石中含有游离态铁,但陨石不算自然界,故错误;
⑤钠最外层电子少,易失去,易被氧化,从而性质活泼,在自然界中只能以化合物的形式存在,故正确;
故选D.
点评 本题考查了游离态、化合态的含义,元素在自然界中的存在状态与元素的活泼性有密切的关系,活泼元素在自然界中以化合物的形式存在,不活泼的元素在自然界中以单质的形式存在,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题

 ⑤
⑤ ⑥HOCH2CH2CH2COOH
⑥HOCH2CH2CH2COOH查看答案和解析>>
科目:高中化学 来源: 题型:多选题
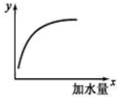 如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )| A. | c(H+)或 c(OH-) | B. | HA的电离平衡常数Ka | ||
| C. | c(H+)/c(HA) | D. | n(H+)或 n(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3kJ/mol | |
| B. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-57.3kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$ O2 (g)═8CO2 (g)+9H2O(g)△H=-5518 kJ/mol | |
| D. | 2C8H18(g)+25O2 (g)═16CO2 (g)+18H2O(1)△H=-5518 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
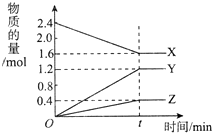 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示.反应在t时刻达到平衡,据图回答下列问题:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示.反应在t时刻达到平衡,据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.4mol•L-1 | B. | 1.2mol•L-1 | C. | 1.1mol•L-1 | D. | 1.0mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁与氢碘酸反应:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| C. | FeBr2溶液中通入足量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2++4Cl- | |
| D. | 向FeCl2溶液中加入少量K3[Fe(CN)6]溶液:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com