
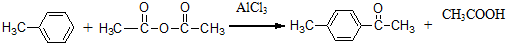
 .
.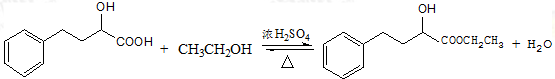 .
. .
.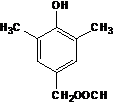 或
或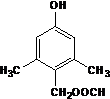 .
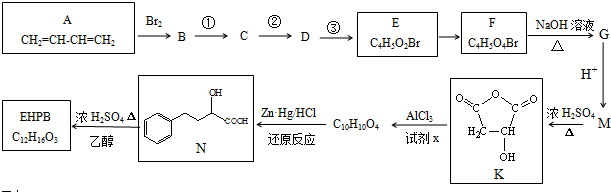
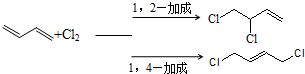
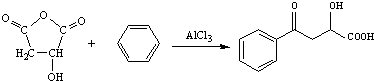
.分析 由K的结构简式逆推可知M为 ,G为NaOOCCH2CH(OH)COONa,根据F的分子式可知F的结构简式为HOOCCH2CHBrCOOH,1molE发生银镜反应可生成4molAg,即E中含有两个醛基,所以E为OHCCH2CHBrCHO,则A与溴发生1,4-加成生成B为BrCH2CH=CHCH2Br,B发生碱性水解反应得到C为HOCH2CH=CHCH2OH,C与溴化氢加成得到D为HOCH2CH2CHBrCH2OH,D发生氧化反应得到E,比较K和C10H10O4的分子式,结合N的结构可知试剂a为苯,C10H10O4为
,G为NaOOCCH2CH(OH)COONa,根据F的分子式可知F的结构简式为HOOCCH2CHBrCOOH,1molE发生银镜反应可生成4molAg,即E中含有两个醛基,所以E为OHCCH2CHBrCHO,则A与溴发生1,4-加成生成B为BrCH2CH=CHCH2Br,B发生碱性水解反应得到C为HOCH2CH=CHCH2OH,C与溴化氢加成得到D为HOCH2CH2CHBrCH2OH,D发生氧化反应得到E,比较K和C10H10O4的分子式,结合N的结构可知试剂a为苯,C10H10O4为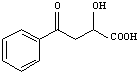 ,N与乙醇发生酯化反应生成EHPB为
,N与乙醇发生酯化反应生成EHPB为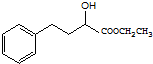 .
.
解答 解:由K的结构简式逆推可知M为 ,G为NaOOCCH2CH(OH)COONa,根据F的分子式可知F的结构简式为HOOCCH2CHBrCOOH,1molE发生银镜反应可生成4molAg,即E中含有两个醛基,所以E为OHCCH2CHBrCHO,则A与溴发生1,4-加成生成B为BrCH2CH=CHCH2Br,B发生碱性水解反应得到C为HOCH2CH=CHCH2OH,C与溴化氢加成得到D为HOCH2CH2CHBrCH2OH,D发生氧化反应得到E,比较K和C10H10O4的分子式,结合N的结构可知试剂a为苯,C10H10O4为
,G为NaOOCCH2CH(OH)COONa,根据F的分子式可知F的结构简式为HOOCCH2CHBrCOOH,1molE发生银镜反应可生成4molAg,即E中含有两个醛基,所以E为OHCCH2CHBrCHO,则A与溴发生1,4-加成生成B为BrCH2CH=CHCH2Br,B发生碱性水解反应得到C为HOCH2CH=CHCH2OH,C与溴化氢加成得到D为HOCH2CH2CHBrCH2OH,D发生氧化反应得到E,比较K和C10H10O4的分子式,结合N的结构可知试剂a为苯,C10H10O4为 ,N与乙醇发生酯化反应生成EHPB为
,N与乙醇发生酯化反应生成EHPB为 .
.
(1)E为OHCCH2CHBrCHO,含氧官能团为醛基,故答案为:醛基;
(2)a.①为卤代烃的水解反应反应,反应试剂和条件是:NaOH水溶液、加热,故答案为:NaOH水溶液、加热;
b.②、③的反应类型依次是加成反应、氧化反应,
故答案为:加成反应;氧化反应;
(3)G为NaOOCCH2CH(OH)COONa,F的结构简式为HOOCCH2CHBrCOOH,羧基、溴原子能与氢氧化钠发生反应,1molF转化成G所消耗的NaOH的物质的量为3molmol,
故答案为:3;
(4)M的结构简式为 ,
,
故答案为: ;
;
(5)①EHPB不能与NaHCO3反应,有机物N→EHPB的化学方程式为: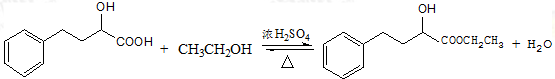 ,
,
故答案为: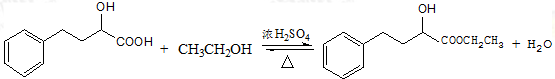 ;
;
②有机物K与试剂x发生反应的化学方程式为 ,
,
故答案为: ;
;
(6)有机物N有多种同分异构体,一种满足下列条件的同分异构体;a.含有酚羟基,说明含有酚羟基与苯环;b.既能水解又能发生银镜反应,含有甲酸形成的酯基;c.苯环上的一氯代物只有一种,苯环上有1种H原子;d.核磁共振氢谱有5组峰,符合条件的结构简式为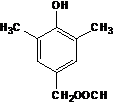 或
或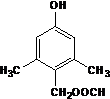 ,
,
故答案为: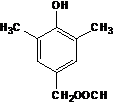 或
或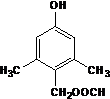 .
.
点评 本题考查有机物的推断与合成,是对有机物知识的综合考查,综合性较强,能较好的考查学生的阅读、分析与思维能力,熟练掌握官能团的性质与转化.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH | |
| B. | 图2表示 KNO3的溶解度曲线,a点所示的溶液是80℃时KNO3的不饱和溶液 | |
| C. | 图3 表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| D. | 图4表示恒温恒容条件下,2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验内容 | 实验目的 |
| A | 测同温同浓度下的Na2CO3和Na2SO3水溶液的pH | 确定碳和硫两元素非金属性强弱 |
| B | 向CH2=CHCH2OH中滴加酸性KMnO4溶液 | 证明CH2=CHCH2OH中含有碳碳双键 |
| C | 取久置的Na2SO3溶于水,加硝酸酸化的BaCl2溶液 | 证明Na2SO3部分被氧化 |
| D | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入足量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 | 检验蔗糖水解产物具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. .
.
 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
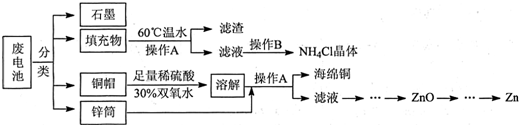
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
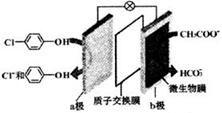 利用微生物电池处理含乙酸钠和对氯酚(
利用微生物电池处理含乙酸钠和对氯酚( )的废水,工作原理如图所示.下列说法正确的是( )
)的废水,工作原理如图所示.下列说法正确的是( )| A. | 电极b是正极 | B. | 质子从a极移向b极 | ||
| C. | 处理后的废水pH升高 | D. | a极的电极反应式: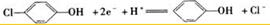 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com