
【题目】碳、氮及其化合物广泛存在于自然界中,回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主,原因是__________。
(2)CS2分子中,共价键的类型有_______ , C原子的杂化轨道类型是______,写出两个与CS2具有相同空间构型的分子或离子_______。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是______;
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(g)+ N2H4(g)=2N2(g)+4H2O(g) △H=-1038.7kJ/mol。若该反应中有4molN-H键断裂,则形成的π键有___mol。
③肼能与硫酸反应生成N2H6SO4, N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在____ (填标号)。
a.离子键 b.共价键 c.配位键 d.范德华力
(4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图29所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为______。其晶胞参数(晶胞边长)为1.4nm,晶体密度为____g/cm3。
【答案】 碳原子最外层有4个电子,不容易得或失电子形成稳定结构 π、δ sp CO2、SCN- 三角锥形 3 d K3C60 2
【解析】(1)共价键为原子之间以共用电子对成键,碳原子核外有4个电子,且元素的非金属性较弱,但半径较小,反应中难以失去或得到电子形成稳定结构;
(2)CS2分子的结构式为S=C=S,含有δ键和π键,CS2分子中C原子形成2个δ键,孤对电子数为![]() =0,则为sp杂化;等电子体具有相似的结构,CO2、SCN-与CS2是等电子体,则具有相同空间构型;
=0,则为sp杂化;等电子体具有相似的结构,CO2、SCN-与CS2是等电子体,则具有相同空间构型;
(3)①NH3分子中氮原子含有3个共价键和一个孤电子对,所以空间构型是三角锥型;
②N2O4+2N2H4═3N2+4H2O,若该反应中有4mol N-H键断裂,即有1mol N2H4参加反应,生成1.5mol N2,形成π键的物质的量为2×1.5mol=3mol;
③肼与硫酸反应的离子方程式为N2H4+2H+═N2H62+,N2H6SO4晶体类型与硫酸铵相同,N2H62+中的化学键是共价键与配位键,N2H62+与SO42-之间是离子键,不存在范德华力,故答案为d;
(4)K位于棱和体心,晶胞中的个数为12×![]() +9=12,C60位于定点和面心,个数为8×
+9=12,C60位于定点和面心,个数为8×![]() +6×
+6×![]() =4,化学式为K3C60,则晶胞的质量为
=4,化学式为K3C60,则晶胞的质量为![]() g,其晶胞参数为1.4nm=1.4×10-7cm,则体积为(1.4×10-7)3cm3,所以密度为
g,其晶胞参数为1.4nm=1.4×10-7cm,则体积为(1.4×10-7)3cm3,所以密度为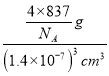 =2.0gcm-3。
=2.0gcm-3。


科目:高中化学 来源: 题型:
【题目】对于可逆反应A(g)+3B(s)![]() 2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A、υ(A)=0.5mol/(L·min) B、υ(B)=1.2mol/(L·s)
C、υ(C)=0.1mol/(L·s) D、υ(D)=0.4mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下的密闭容器中存在如下反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)达到平衡时,CO的转化率为多少?
(3)当CO的起始浓度仍为2mol·L-1,H2O(g)的起始浓度为6mol·L-1,求平衡时CO的转化率?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
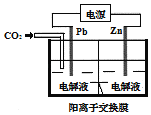
A. Pb与电源的正极相连
B. ZnC2O4在离子交换膜右侧生成
C. 正极反应式为:Zn﹣2e﹣═Zn2+
D. 标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述错误的是
A. 回收的地沟油可以用来制造肥皂、提取甘油或生产生物柴油
B. 纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体
C. 纤维素属于多糖,但不是人类的营养物质
D. 绿色化学的核心是应用化学原理从源头上减少和消除工业生产对环境的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料是人类社会发展的重要物质基础。下列说法正确的是
A.钛及钛合金是目前使用量最大的金属材料
B.镁是一种国防金属,电解熔融MgCl2可得到单质镁
C.珠港澳大桥为了防腐蚀可以在钢铁中增加含碳量
D.稀土(钇、钪及镧系)是战略金属,稀土元素均位于ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2 , 通过计算回答:用双线桥标出反应中电子转移的方向和数目 , 参加反应的HCl的物质的量为 , 其中被氧化的HCl的质量 .
MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2 , 通过计算回答:用双线桥标出反应中电子转移的方向和数目 , 参加反应的HCl的物质的量为 , 其中被氧化的HCl的质量 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com