
| A£® | ČōŅŖČ·¶ØČÜŅŗXÖŠŹĒ·ńŗ¬ÓŠFe3+£¬Ęä²Ł×÷ĪŖȔɣĮæŌČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėŹŹĮæKSCNČÜŅŗ£¬ČÜŅŗ±äŃŖŗģÉ«£¬Ōņŗ¬ÓŠFe3+ | |
| B£® | ³ĮµķCĪŖBaSO4£¬³ĮµķHĪŖBaCO3£¬¹¤ŅµÉĻĶłBaCO3ÖŠ¼ÓČė±„ŗĶµÄNa2CO3æÉŅŌŹµĻÖBaSO4µÄ×Ŗ±ä | |
| C£® | ČÜŅŗÖŠŅ»¶Øŗ¬ÓŠH+”¢Al3+”¢NH4+”¢Fe2+”¢SO42-”¢Cl- | |
| D£® | ČōČÜŅŗXĪŖ100 mL£¬²śÉśµÄĘųĢåAĪŖ112 mL£Ø±źæö£©£¬ŌņXÖŠc£ØFe2+£©=0.05 mol•L-1 |
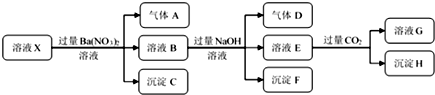
·ÖĪö ŌŚĒæĖįŠŌČÜŅŗÖŠŅ»¶Ø²»»į“ęŌŚCO32-”¢SO32-Ąė×Ó£»¼ÓČė¹żĮæĻõĖį±µÉś³É³Įµķ£¬ŌņøĆ³ĮµķCĪŖBaSO4£¬ĖµĆ÷ČÜŅŗÖŠŗ¬ÓŠSO42-Ąė×Ó£¬Éś³ÉĘųĢåA£¬ŌņAÖ»ÄÜŹĒNO£¬ĖµĆ÷ČÜŅŗÖŠŗ¬ÓŠ»¹ŌŠŌĄė×Ó£¬ŌņŅ»¶ØĪŖFe2+Ąė×Ó£¬ČÜŅŗBÖŠ¼ÓČė¹żĮæNaOHČÜŅŗ£¬³ĮµķFÖ»ĪŖFe£ØOH£©3£¬Éś³ÉĘųĢåD£¬ŌņDĪŖNH3£¬ĖµĆ÷ČÜŅŗÖŠŗ¬ÓŠNH4+Ąė×Ó£»ČÜŅŗEÖŠĶØČėCO2ĘųĢå£¬Éś³É³ĮµķH£¬ŌņHĪŖAl£ØOH£©3£¬EĪŖNaOHŗĶNaAlO2£¬ĖµĆ÷ČÜŅŗÖŠŗ¬ÓŠAl3+Ąė×Ó£¬ŌŁøł¾ŻĄė×Ó¹²“ęÖŖŹ¶£¬ČÜŅŗÖŠŗ¬ÓŠFe2+Ąė×Ó£¬ŌņŅ»¶Ø²»ŗ¬NO3-Ąė×ÓŗĶSO32-Ąė×Ó£¬ÄĒĆ“Ņ»¶Øŗ¬ÓŠSO42-Ąė×Ó£¬ÄĒĆ“¾ĶŅ»¶Ø²»ŗ¬Ba2+Ąė×Ó£¬²»ÄÜČ·¶ØŹĒ·ńŗ¬ÓŠµÄĄė×ÓFe3+ŗĶCl-£¬ŅŌ“Ė½ųŠŠ½ā“š£®
½ā“š ½ā£ŗŅĄ¾Ż·ÖĪöæÉÖŖ£ŗČÜŅŗÖŠŅ»¶Ø“ęŌŚ£ŗNH4+”¢Al3+”¢Fe2+”¢SO42-£¬Ņ»¶Ø²»ŗ¬ÓŠ£ŗBa2+”¢CO32-”¢SO32-”¢NO3-£¬²»ÄÜČ·¶ØŹĒ·ńŗ¬ÓŠ£ŗFe3+ŗĶCl-£¬
A”¢øł¾ŻÉĻŹöĮ¬ŠųŹµŃé²»ÄÜČ·¶ØČÜŅŗXÖŠŹĒ·ńŗ¬ÓŠFe3+£¬ČōŅŖČ·¶ØČÜŅŗXÖŠŹĒ·ńŗ¬ÓŠFe3+£¬Ęä²Ł×÷ĪŖȔɣĮæŌČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėŹŹĮæKSCNČÜŅŗ£¬ČÜŅŗ±äŃŖŗģÉ«£¬Ōņŗ¬ÓŠFe3+£¬¹ŹAÕżČ·£»
B”¢øł¾ŻÉĻŹö·ÖĪöæÉÖŖ³ĮµķCĪŖBaSO4£¬HĪŖAl£ØOH£©3£¬BaCO3Óė¹żĮæµÄ¶žŃõ»ÆĢ¼Éś³ÉĢ¼ĖįĒā±µ£¬Ņ×ČÜÓŚĖ®£¬¹ŹB“ķĪó£»
C”¢ŅĄ¾Ż·ÖĪöæÉÖŖ£¬ČÜŅŗÖŠŅ»¶Ø“ęŌŚ£ŗNH4+”¢Al3+”¢Fe2+”¢SO42-£¬²»ÄÜČ·¶ØCl-ŹĒ·ń“ęŌŚ£¬¹ŹC“ķĪó£»
D”¢Éś³ÉĘųĢåAµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ£ŗ3Fe2++NO3-+4H+=3Fe3++NO”ü+2H2O£¬²śÉśµÄĘųĢåAĪŖ112 mL£¬ĪļÖŹµÄĮæĪŖ£ŗ$\frac{0.112L}{22.4L/mol}$=0.005mol£¬¹Źn£ØFe2+£©=3”Į0.005=0.015mol£¬c£ØFe2+£©=$\frac{0.015mol}{0.1L}$=0.15mol/L£¬¹ŹD“ķĪó£¬
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖ³£¼ūŅõŃōĄė×ӵļģŃ锢ĪŽ»śĶʶĻ£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāÕĘĪÕ³£¼ūĄė×ӵĊŌÖŹ¼°¼ģŃé·½·Ø£¬ŹŌĢā³ä·Öæ¼²éĮĖѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°Įé»īÓ¦ÓĆĖłŃ§ÖŖŹ¶µÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ca | B£® | Li | C£® | K | D£® | Na |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņ»¶ØĢõ¼žĻĀÓėĒāĘų·“Ó¦ | B£® | Óė×ćĮæµÄŅŗäå·“Ó¦ | ||
| C£® | ŌŚµ¼¹ÜæŚµćČ¼ | D£® | ĶØČė×ćĮæäåĖ®ÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖįŠŌ£ŗHF£¾HCl£¾H2S | B£® | ·Šµć£ŗCBr4£¾CCl4£¾CF4 | ||
| C£® | ¼īŠŌ£ŗCa£ØOH£©2£¾Mg£ØOH£©2£¾Al£ØOH£©3 | D£® | ĪČ¶ØŠŌ£ŗH2O£¾H2S£¾H2Se |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£® £®
£®
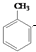 µ½DµÄŗĻ³ÉĀ·ĻߣØĪŽ»śŹŌ¼ĮČĪŃ”£¬ÓĆŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼±ķŹ¾£©£®
µ½DµÄŗĻ³ÉĀ·ĻߣØĪŽ»śŹŌ¼ĮČĪŃ”£¬ÓĆŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼±ķŹ¾£©£®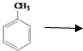 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µĪČė·ÓĢŖČÜŅŗ±äŗģ£¬ŌŁ¼ÓČėH2SO4ČÜŅŗŗģÉ«ĶĖČ„ | |
| B£® | µĪČė·ÓĢŖČÜŅŗ±äŗģ£¬ŌŁ¼ÓČėĀČĖ®ŗóŗģÉ«ĶĖČ„ | |
| C£® | µĪČė·ÓĢŖČÜŅŗ±äŗģ£¬ŌŚ¼ÓČėBaCl2ČÜŅŗŗó²śÉś³ĮµķĒŅŗģÉ«ĶĖČ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ©Ģž¹ŁÄÜĶŵĽį¹¹Ź½£ŗC=C | B£® | Č©»łµÄ½į¹¹¼ņŹ½£ŗHOC- | ||
| C£® | Ēā·Ö×ÓÖŠ¹²ÓƵē×Ó¶ŌµÄ¹ģµĄ±ķŹ¾£ŗ | D£® | ±ūĖįµÄ½į¹¹¼ņŹ½£ŗCOOHCH2CH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | COŗĶN2 | B£® | O3ŗĶSO2 | C£® | N2H4ŗĶC2H4 | D£® | CO2ŗĶN2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com