
下列各组物质属于同系物的是( )
A. 2,2-二甲基丙烷和新戊烷 B.2,2-二甲基-1-丙醇和2-甲基-1-丁醇
C.对氯甲苯和邻氯乙苯 D.甲基丙烯酸和甲酸丁酯
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源:2015-2016学年四川省高二下期中化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g)△H1=—99kJ.mol-1,
CH3OH(g)△H1=—99kJ.mol-1,
②CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H2=—58kJ.mol-1
CH3OH(g)+H2O(g)△H2=—58kJ.mol-1
③CO2(g)+H2(g) CO(g)+H2O(g)△H3
CO(g)+H2O(g)△H3
回答下列问题:
(1)写出CO2的结构式__________。
(2)由上述数据计算出△H3=kJ.mol-1
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,温度T1、T2对反应的影响,下列正确的是__________(填序号)
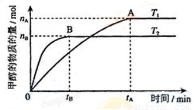
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tAmol/(L·min)
②该反应在T1时的平衡常数比T2时的小
③当生成1mol甲醇的同时,生成1molCO2,说明反应达到平衡
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;该温度条件下,反应平衡常数为__________(计算出结果)
(5)在直接以甲醇为燃料电池中,电解质溶液为硫酸性,负极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古杭锦后旗奋斗中学高一下期中化学卷(解析版) 题型:选择题
下列关于元素周期表和元素周期律的说法错误的是( )
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,非金属性逐渐增强
C.因为Na比K容易失去电子,所以Na比K的还原性强
D.O与S为同主族元素,且O比S的非金属性强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二5月月考化学试卷(解析版) 题型:选择题
将甲烷、氧气、过氧化钠置于密闭容器中,在150 0C时用电火花点燃,充分反应后容器内压强为零,则甲烷、氧气、过氧化钠的物质的量之比为( )
A.1:2:3 B.2:1:6 C. 2:1:3 D. 1:2:6
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二5月月考化学试卷(解析版) 题型:选择题
某气态烃0.5mol能与1mol HCl氯化氢完全加成,加成产物分子上的氢原子又可被3mol Cl2取代,则气态烃可能是( )
A.CH ≡CH B.CH2=CH2 C. CH2=C(CH3)CH3 D.CH≡C—CH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽师大附中高二下期中化学试卷(解析版) 题型:填空题
短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B原子的最外层电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为___________________;
(2)已知:①E-E→2E•;△H=+a kJ•mol-1
②2A•→A-A;△H=-b kJ•mol-1
③E•+A•→A-E;△H=-c kJ•mol-1(“•”表示形成共价键所提供的电子)
写出298K时,A2与E2反应的热化学方程式___________________;
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)?X(g);△H=-d J•mol-1(d>0,X为A、B、C三种元素组成的一种化合物).初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2mol A2、1mol BC | 1mol X | 4mol A2、2mol BC |
平衡时n(X) | 0.5mol | n2 | n3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
体系的压强 | P1 | P2 | P3 |
反应物的转化率 | α1 | α2 | α3 |
①该温度下此反应的平衡常数K的值为_____;
②三个容器中的反应分别达平衡时各组数据关系正确的是_____(填序号)
A.α1+α2=1 B.α3<α1 C.n2<n3<1.0mol D.P3<2P1=2P2 E.Q1+Q2=d F.Q3=2Q1
(4)在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为65.5%,请在下图中画出第5min到新平衡时X的物质的量浓度的变化曲线。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽师大附中高二下期中化学试卷(解析版) 题型:选择题
恒温下,容积为2L的定容密闭容器中,充入3molA、ymolB,发生反应:3A(g)+2B(g) 2C(g)+xD(g)。2min后达到平衡,测得从反应开始到平衡时C的速率为0.3mol·L-1·min-1.下列推断的结论正确的是
2C(g)+xD(g)。2min后达到平衡,测得从反应开始到平衡时C的速率为0.3mol·L-1·min-1.下列推断的结论正确的是
A.y 1.2
1.2
B.增大反应体系的压强,反应速率不一定增大
C.v正(A)>v逆(C),不可能为平衡状态
D.混合气体的密度不再变化,一定为平衡状态
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期中化学试卷(解析版) 题型:填空题
分析下图有机分子的球棍模型,回答下列问题:
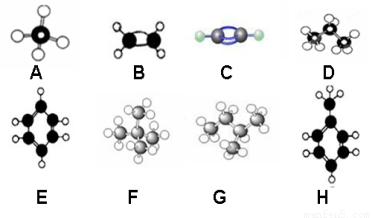
(1)互为同分异构体的是__________,E和H互为 ,E的分子空间构型是 。 (2)F与氯气发生一元取代反应的化学方程式 。
(3)有机物种类繁多的原因有 、 (答两种原因)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列设计的实验方案能达到实验目的的是
A. 将苯和溴水混合后加入Fe粉制溴苯
B. 为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,振荡,若无油滴浮在液面上,说明油脂已完全反应
C. 检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热煮沸,观察是否出现红色沉淀
D. 探究化学反应的限度:取5ml 0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5-6滴,充分反应,根据溶液中是否含有碘单质和碘离子判断该反应有一定限度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com