
聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛应用于制作光导纤维。已知A为某种聚甲基丙烯酸酯纤维的单体,其转化关系如下:
(1)A的结构简式为 。
(2)下列有关E的说法不正确的是 (填写字母编号)
A.能使酸性高锰酸钾溶液褪色 B.能使溴的CCl4溶液褪色
C.一定条件下,能够发生消去反应 D.一定条件下,能够发生取代反应
(3)F的同分异构体中属于酯类的有 种
(4)反应②的化学方程式是
反应⑤的化学方程式是
 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
在混合体系中,确认化学反应先后顺序有利于问题的解决,下列反应先后顺序判断正确的是
A.在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+
B.在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:Fe3+、Cu2+、H+、Fe2+
C.在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3、K2CO3
D.在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
平衡是化学反应原理中的重要内容。按要求回答下列问题:
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH1 平衡常数为K1
2SO3(g) ΔH1 平衡常数为K1
2NO(g)+O2(g) 2NO2(g) ΔH2 平衡常数为K2
2NO2(g) ΔH2 平衡常数为K2
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的
SO3(g)+NO(g)的
 ΔH=______ (用ΔH 1和ΔH 2表示);此反应该温
ΔH=______ (用ΔH 1和ΔH 2表示);此反应该温
度下的平衡常数K=______(用K1和K2表示)。
(2)已知A(g)+B(g)  C(g)+D(g),该反应在
C(g)+D(g),该反应在
3L密闭容器中,在两种不同的条件下进行反应,
A、B的起始物质的是分别为3.0mol和6.0mol,
其中实验I的条件为T1℃。A的物质的量随时间
的变化如图所示。
①实验Ⅱ可能改变的条件是_______________。
②T1℃时该反应的平衡常数为_____(用分数表
示),达到平衡时,A的反应速率为____。
(3)已知HCN溶液的电离平衡常数Ka=10-5 mol•L-1,c平衡(HCN)≈c起始(HCN),水的电离可不计,则此温度下0.1 mol•L-1的HCN溶液的pH=_________。
(4)对于0.1mol•L-1 Na2CO3溶液,该溶液中离子浓度由大到小的顺序是______,向该溶液中加水稀释的过程中,c(H2CO3)逐渐____(填“增大”“不变”或“减小”, 下同) ,c(H2CO3)/ c(CO32-)逐渐______。
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是某只含有C、H、O、N的有机物简易球棍模型,下列关于该有机物的说法正确的是( )
A.分子式为C3H7NO
B.在一定条件下,可以通过聚合反应,生成高分子化合物
C.不能和盐酸溶液反应
D.不能和NaHCO3溶液反应生成CO2

查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是
A.E可能是一种金属元素 B.在ECln中E与Cl之间形成共价键
C.E位于元素周期表的IVA族 D.E的一种氧化物为EO
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
将0.2mol/L HCN溶液和0.1mol/L NaOH溶液等体积混合后溶液呈碱性,下列关系式中不正确的是
A. c(HCN) >c(CN—) B. c(Na+)>c(CN—)
C. c(HCN)-c(CN—)=c(OH—) D. c(HCN)+c(CN—)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二12月月考化学试卷(解析版) 题型:填空题
(7分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
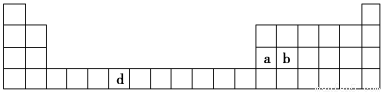
(1)请写出元素d的基态原子电子排布式________________________________________。
(2)b元素的氧化物中b与氧元素之间的共价键类型是________。其中b原子的杂化方式是_______。
(3)a单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若已知a的原子半径为d,NA代表阿伏加德罗常数,a的相对原子质量为M,则一个晶胞中a原子的数目为________,该晶体的密度为________(用字母表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com