
| A����ⷨ����ͭ���������������� 64g ʱ�����·ͨ��������Ϊ 2NA |
| B��25��ʱ��1LpH=3 �Ĵ�����Һ�к��д������������ 0.001NA |
| C��1L0.1 mol?L-1NaClO ��Һ�к� ClO-��ĿΪ 0.1NA |
| D����֪ N2��g��+3H2��g��?2NH3��g����H=-92.2kJ?mol-1������Ӧ����73.76kJʱ�����γ� H-H �� 2.4NA |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Ȼ�� | B����������� |
| C�����ˮ | D���廯������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
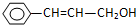 Ϊij�л���A�Ľṹ�����ڸ����ʵ����ʣ�����˵����ȷ���ǣ�������
Ϊij�л���A�Ľṹ�����ڸ����ʵ����ʣ�����˵����ȷ���ǣ�������| A���٢ڢ� | B���ܢݢ� |
| C���٢ڢܢݢ� | D��ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ�£�8gO2����4NA������ |
| B��l L 0.1 mol?L-1�İ�ˮ�к���0�� 1NA��NH+4 |
| C����״���£�22.4 L���Ậ��NA��lHC1���� |
| D��1 mol Na����ȫ��������Na2O2��ʧȥ2NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

A�����ʱ������Ӧ�Ļ�ѧ����ʽΪ��2HCl
| ||||
| B����NaClO2��Һ��ȡ0.6mol ClO2ʱ����������0.1mol NCl3 | ||||
| C���������Ļ������ͨ��ʢ�м�ʯ�ҵĸ������Գ�ȥClO2�е� NH3 | ||||
| D����ҺX�ijɷ�ΪNaClO3��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��N2O��NO2 |
| B��O3��SO2 |
| C��CH4��NH3 |
| D��OH-��NH2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ HClO4��HBrO4��HIO4 |
| B������ Ba��OH��2��Ca��OH��2��Mg��OH��2 |
| C����ԭ�� F-��Cl-��Br- |
| D���ȶ��� HCl��H2S��PH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t/s | 2 | 4 | 7 | 9 |
| n��Y��/mol | 0.12 | 0.10 | 0.09 | 0.09 |
| A����Ӧǰ2s��ƽ������v��Z��=2.0��10-3 mol/��L?s�� |
| B�������������䣬����һ������Y����Ӧ����һ���ӿ� |
| C����Ӧ����4sʱ��X��ת����75% |
| D����Ӧ�ﵽƽ��ʱ��X�����ʵ���Ũ��Ϊ0.02mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ǻ����л���һ�����ڴ��� |
| B����������ͬ��������һ��ѡ���̼����Ϊ���� |
| C�������ܷ�����ȥ��Ӧ |
| D�������ܷ���ȡ����Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com