
| 1 |
| 10 |
| n |
| c |
| 2.009g |
| 143.5g/mol |
| 0.14mol-0.1mol |
| 2 |
| 0.04mol |
| 3 |
| ||
| 0.5mol/L |


科目:高中化学 来源: 题型:
| A、Na→NaOH→Na2CO3→NaCl |
| B、Fe→FeCl3→Fe(OH)3→Fe2O3 |
| C、Mg→MgCl2→Mg(OH)2→MgSO4 |
| D、Al→Al2O3→Al(OH)3→AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释后,溶液中各离子浓度均变小 | ||||
| B、原溶液中,C(Na+)=C(HCO3-)+C(H2CO3)=0.1mol/L | ||||
C、稀释后,溶液中
| ||||
| D、原溶液加入少量NaOH溶液后,其碱性减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)?c(OH-)<1×10-14 |
| B、c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| C、c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| D、c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、C6H12O6(葡萄糖aq)+6O2
| ||
| B、CH3COOH+KOH?CH3COOK+H2O | ||
| C、反应物的总能量大于生成物的总能量 | ||
| D、破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、置换反应一定属于氧化还原反应 |
| B、离子反应一定属于氧化还原反应 |
| C、有的复分解反应属于氧化还原反应 |
| D、所有化合反应都属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
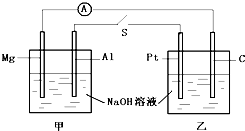 如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )| A、电流计指针不发生偏转 |
| B、Al、Pt两电极有氢气生成 |
| C、Mg、C两电极生成的气体在一定条件下可以恰好完全反应 |
| D、甲池pH减小,乙池pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸中加入碳酸钙:CO32-+2H+═H2O+CO2↑ |
| B、向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com