
(16分)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式,并在方框内填上系数。
□C+□KMnO4+□H2SO4 =□CO2↑+□MnSO4 +□K2SO4+□
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
①实验1条件下,反应从开始至达到平衡,以v(CO2)表示的反应速率为 (保留小数点后二位数,下同)。
②实验2条件下平衡常数K= ,该反应为 (填“吸热”或“放热”)反应。
(3)已知在常温常压下:
①2CH3OH(l) +3O2(g)=2CO2(g)+4H2O(g) ΔH1 =-1275.6 kJ/mol
②2CO (g)+ O2(g)=2CO2(g) ΔH2 =-566.0 kJ/mol
③H2O(g)=H2O(l) ΔH3 =-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式: 。
(4)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。

该电池正极的电极反应式为 ;该电池工作时,溶液中的OH-向 (填“正”或“负”)极移动。
(1)5C+4KMnO4 +6 H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O (3分)
(2)①0.13mol/(L·min) (2分) ②0.17(2分); 放热(2分)
(3)CH3OH(l)+O2(g)= CO(g)+2H2O(g) ΔH=-354.8KJ/mol(3分)
(4)①O2 + 4e- + 2 H2O = 4OH—(2分) ②负(2分)
【解析】
试题分析:(1)高锰酸钾中锰元素化合价降低(+7)-(+2)=5价,碳元素化合价升高0-(-4)=4价,化合价升降守恒,所以高锰酸钾前的系数是4,碳单质前的系数是5,根据原子守恒,二氧化碳前是5,硫酸锰前是4,硫酸钾前面是2,根据硫酸跟守恒,所以硫酸前面是6,据氧原子和氢原子守恒,产物少6个水分子,故方程式为:5C+4KMnO4 +6 H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O;(2)①、由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,v(CO)=1.6mol÷2L÷6min=0.13mol/(L·min);速率之比等于化学计量数之比,故v(CO2)=v(CO)=0.13mol/(L?min);③、平衡时CO的物质的量为1.6mol,则可列三段式
CO(g)+ H2O(g)? CO2(g)+ H2(g),
开始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
该反应前后气体体积不变,故利用物质的量代替浓度计算平衡常数,故900℃时该反应平衡常数k=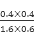 =0.17,则该反应为放热反应(2)已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1)△H=-1275.6kJ/mol,②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol,③ H2O(g)=H2O(l) ΔH3 =-44.0 kJ/mol根据盖斯定律,①-②得2CH3OH(1)+2O2(g)=2CO(g)+4H2O(g),故△H=(-1275.6kJ/mol)-(-566.0kJ/mol)=-709.6 kJ/mol即CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-354.8kJ/mol,(3)①电池反应原理甲醇发生氧化反应,在负极放电,氧气发生还原反应,在正极放电,反应式为O2+4e-+2H2O=4OH-,②负极失电子产生大量正电荷,则该电池工作时,溶液中的OH-向负极。
=0.17,则该反应为放热反应(2)已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1)△H=-1275.6kJ/mol,②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol,③ H2O(g)=H2O(l) ΔH3 =-44.0 kJ/mol根据盖斯定律,①-②得2CH3OH(1)+2O2(g)=2CO(g)+4H2O(g),故△H=(-1275.6kJ/mol)-(-566.0kJ/mol)=-709.6 kJ/mol即CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-354.8kJ/mol,(3)①电池反应原理甲醇发生氧化反应,在负极放电,氧气发生还原反应,在正极放电,反应式为O2+4e-+2H2O=4OH-,②负极失电子产生大量正电荷,则该电池工作时,溶液中的OH-向负极。
考点:化学反应原理。


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期第四次月考理综化学试卷(解析版) 题型:选择题
化学与社会、生产、生活紧切相关,下列说法正确的是
①石英只可用于生产光导纤维,且常温下不与强酸反应;
②次氯酸钠溶液可用于环境的消毒杀菌;
③黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成;
④用铜片在加热的条件下就可鉴别浓硫酸和稀硫酸;
⑤70mL的H2S和90mL的O2混合点燃后恢复到原状况可产生70mL的SO2;
⑥将过量CO2气体通入水玻璃中可生成硅酸和纯碱
A.①②④⑤ B.①②③④ C.②④⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期12月联考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.钾原子结构示意图:
B.水的电子式:
C.CO2的比例模型:
D.间羟基苯甲酸的结构简式:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高三1月模拟考试理综化学试卷(解析版) 题型:填空题
(16分)羰基化反应是制备不饱和酯的有效途径,如:
反应①:
化合物I可由化合物Ⅲ合成:

(1)化合物Ⅱ的分子式为________,化合物Ⅱ在NaOH溶液中完全水解的化学方程式为_________。
(2)化合物Ⅲ的结构简式为________,化合物Ⅳ通过消去反应生成化合物I的化学方程式为______(注明反应条件)。
(3)化合物Ⅴ是化合物Ⅱ的同分异构体,苯环上有两个取代基且能发生银镜反应,Ⅴ的核磁共振氢谱除苯环峰外还有两组峰,峰面积之比为1︰2,Ⅴ的结构简式为_________(写一种即可)。
(4)聚合物 单体的结构简式为_________。用类似反应①的方法,利用丙炔与合适的原料可以合成该单体,化学方程式为________。
单体的结构简式为_________。用类似反应①的方法,利用丙炔与合适的原料可以合成该单体,化学方程式为________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高三1月模拟考试理综化学试卷(解析版) 题型:选择题
设nA为阿伏加德罗常数的数值,下列说法正确的是
A.1 mol甲烷中含有10nA个质子
B.27g铝被完全氧化成氧化铝,失去2nA个电子
C.标准状况下,22.4 L苯含有nA个C6H6分子
D.常温常压下,28g乙烯含有2nA个碳碳双键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三一轮复习基础知识检测化学试卷(解析版) 题型:选择题
在不同温度下,水达到电离平衡时c(H+)与c(OH-)的关系如图所示,下列说法中正确的是

A.100℃,pH=12的NaOH和pH=2的H2SO4溶液恰好中和,所得溶液的pH等于7
B.25℃,0.2 mol/L Ba(OH)2和0.2 mol/L HCl溶液等体积混合,所得溶液的pH等于7
C.25℃,0.2 mol/L NaOH与0.2 mol/L乙酸溶液恰好中和,所得溶液的pH等于7
D.25℃,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液的pH大于7
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三一轮复习基础知识检测化学试卷(解析版) 题型:选择题
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:2FeCl3+2HI=2FeCl2+I2+2HCl;2Co(OH)3+6HCl =2CoCl2+Cl2↑+6H2O
2Fe(OH)2+ I2+2KOH = 2Fe(OH)3+2KI; 3I2+6KOH=5KI+KIO3+3H2O
复分解反应:2HSCN +K2CO3 = 2KSCN + CO2 ↑ + H2O;
KCN + CO2 + H2O = HCN + KHCO3
热分解反应:4NaClO 3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是
A.氧化性(酸性溶液):FeCl3 > Co(OH)3 > I2
B.还原性(碱性溶液):Fe(OH)2 > I2 > KIO3
C.热稳定性:NaCl > NaClO4 > NaClO
D.酸性(水溶液):HSCN > H2CO3 > HCN
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省襄阳市四校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列各组离子在无色水溶液中能大量共存的是
A.Na+ Mg2+ Cl- OH- B.MnO4- HCO3- OH- K+
C.Fe3+ H+ SO42- CH3COO- D.K+ NO3- CO32- Na+
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省吉林市高一上学期期末考试化学试卷(解析版) 题型:填空题
(10分)
(1)在Cl2、NO、SO2、NO2、NH3五种气体中,与空气相遇立即变色的是 ,常用于自来水杀菌、消毒的是 ,能用向下排空气法收集的是 ,溶于水后能生成强酸的是 。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒消毒剂。
①工业上通过下列方法制取ClO2,完成该反应的化学方程式:2KClO3 + SO2 =2C1O2+
②配平下列化学方程式:KClO3+ H2C2O4+ H2SO4= ClO2↑+ K2SO4+ CO2↑+ H2O
下列有关上述反应的说法正确的是 。
A.H2C2O4在反应中被还原 B.KClO3是氧化剂
C.ClO2是还原剂 D.生成1molClO2有2mol电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com