
| A. | 用石墨电极电解Ca(NO3)2溶液,当转移电子数为0.2 NA时,阴极析出4 g金属 | |
| B. | 0.1 mol24Mg32S晶体中所含中子总数为2.8 NA | |
| C. | 常温下含有NA个NO2、N2O4分子的混合气体,温度降至标准状况,其体积约为22.4 L | |
| D. | 在熔融状态下,1 mol NaHSO4完全电离出的阳离子数目为2 NA |
分析 A、钙离子不能在溶液中放电;
B、24Mg32S晶体中含28个中子;
C、NO2气体中存在平衡:2NO2?N2O4;
D、在NaHSO4熔融状态下电离为钠离子、硫酸氢根离子.
解答 解:A、钙离子不能在溶液中放电,在阴极上放电的是氢离子而不是钙离子,故A错误;
B、24Mg32S晶体中含28个中子,故0.1mol24Mg32S晶体中含2.8NA个,故B正确;
C、NO2气体中存在平衡:2NO2?N2O4,反应放热,当降温时,平衡右移,气体的物质的量小于1mol,则体积小于22.4L,故C错误;
D、在NaHSO4熔融状态下电离为钠离子、硫酸氢根离子,故1mol硫酸氢钠在熔融状态下电离出NA个阳离子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 实验室配制FeCl3溶液时,需将FeCl3 (s)溶解在较浓盐酸中,然后加水稀释 | |
| B. | 反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应△H>0,△S<0 | |
| C. | 0.1mol•L-1NH4Cl溶液加水稀释,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$的值增大 | |
| D. | 反应CH3COOCH3+H2O?CH3COOH+CH3OH△H>0,达到平衡时,加入少量固体NaOH,则乙酸甲酯水解转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| B. | 通常状况下,NA 个CO2分子的摩尔质量是44g | |
| C. | 物质的量浓度为1mol/L的MgCl2溶液中,含有Cl-个数为2NA | |
| D. | 标准状况下,22.4LH2O含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 镁粉中含少量铝粉:加足量氢氧化钠溶液充分搅拌后过滤 | |
| B. | 碳酸钠溶液中含少量碳酸氢钠:加足量澄清石灰水 | |
| C. | 氯气中混有得氯化氢气体杂质:饱和食盐水 | |
| D. | 硫酸铁溶液中混有硫酸亚铁溶液:通入氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

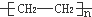 ,
,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com