
【题目】锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示。下列说法正确的是( )
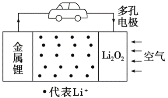
A.电解液中,Li+由多孔电极迁移向锂电极
B.该电池放电时,负极发生了还原反应
C.充电时,电池正极的反应式为Li2O2-2e-=2Li++O2↑
D.电池中的电解液可以是有机电解液或稀盐酸等
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】蛇纹石矿可以看做是由MgO、![]() 、
、![]() 、
、![]() 组成.由蛇纹石制取碱式碳酸镁的实验步骤如下:
组成.由蛇纹石制取碱式碳酸镁的实验步骤如下:

氢氧化物 |
|
|
|
开始沉淀pH |
|
|
|
(1)蛇纹石矿加盐酸溶解后,溶液里除了![]() 外,还含有的金属离子是 ______
外,还含有的金属离子是 ______
(2)进行Ⅰ操作时,控制溶液![]() 有关氢氧化物沉淀的pH见上表
有关氢氧化物沉淀的pH见上表![]() 不能过量,若
不能过量,若![]() 过量可能会导致 ______ 溶解、 ______ 沉淀生成.
过量可能会导致 ______ 溶解、 ______ 沉淀生成.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入 ______ ![]() 填入物质的化学式
填入物质的化学式![]() ,然后 ______
,然后 ______ ![]() 依次填写实验操作名称
依次填写实验操作名称![]() .
.
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是 ______ ![]() 填写物质化学式
填写物质化学式![]() .
.
(5)若热分解不完全,所得碱式碳酸镁中将混有![]() ,则产品中镁的质量分数 ______
,则产品中镁的质量分数 ______ ![]() 填“升高”、“降低”或“不变”,已知碳酸镁的相对分子质量为84,碱式碳酸镁的相对分子质量大于
填“升高”、“降低”或“不变”,已知碳酸镁的相对分子质量为84,碱式碳酸镁的相对分子质量大于![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化硫酰![]() 主要用作氯化剂.它是一种无色液体,熔点
主要用作氯化剂.它是一种无色液体,熔点![]() ,沸点
,沸点![]() ,遇水生成硫酸和氯化氢.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
,遇水生成硫酸和氯化氢.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:![]()
(1)为了提高上述反应中![]() 的平衡转化率,下列措施合理的是 ______
的平衡转化率,下列措施合理的是 ______ ![]() 用编号填空
用编号填空![]() .
.
A.缩小容器体积![]() 使用催化剂
使用催化剂![]() 增加
增加![]() 浓度
浓度![]() 升高温度
升高温度
(2)![]() 时,体积为1L的密闭容器中充入
时,体积为1L的密闭容器中充入![]()
![]() ,达到平衡时容器中含
,达到平衡时容器中含![]()
![]() ,则
,则![]() 时合成
时合成![]() 反应的平衡常数为 ______ .
反应的平衡常数为 ______ .
(3)已知某温度下,已知![]() ,
,![]() ,在
,在![]() 溶于水所得溶液中逐滴加入
溶于水所得溶液中逐滴加入![]() 稀溶液,当
稀溶液,当![]() 浓度为
浓度为![]() 时,浑浊液中
时,浑浊液中![]() 浓度与
浓度与![]() 浓度之比为 ______ .
浓度之比为 ______ .
(4)将(2)所得的平衡混合气溶于足量的![]() 溶液中,计算最终生成沉淀的质量是多少
溶液中,计算最终生成沉淀的质量是多少![]() 写出计算过程
写出计算过程![]() .______ .
.______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取大理石和稀盐酸反应后的废液50g,逐滴加入碳酸钠溶液,根据实验测得的数据绘出右图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量。下列说法正确的是
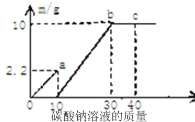
A.图中oa段表示生成的沉淀量
B.c点表示碳酸钠恰好完全反应
C.废液中盐酸的质量分数是7.3%
D.废液中含氯化钙0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列溶液中粒子浓度关系正确的是( )
A.0.01mol·L-1H2S溶液:c(H+)>c(HS-)>c(S2-)>c(H2S)>c(OH-)
B.![]() =10-10的Na2CO3溶液:c(HCO3-)+2c(H2CO3)=c(10-2-10-12)mol·L-1
=10-10的Na2CO3溶液:c(HCO3-)+2c(H2CO3)=c(10-2-10-12)mol·L-1
C.等物质的量的NH4Cl和NaCl的混合溶液:c(NH4)+c(NH3·H2O)+c(Na+)=2c(Cl-)
D.0.1mol·L-1NaHSO3溶液:c(Na+)+c(H+)<c(HSO3-)+c(SO32-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关水溶液的一些叙述正确的是( )
A.某水溶液中,c(H+)=![]() mol/L,该溶液呈中性
mol/L,该溶液呈中性
B.已知电离常数H2CO3的Ka1=4.2×10-7,Ka2=5.6×10-11,HClO的Ka=2.95×10-8,相同温度相同浓度溶液的pH:Na2CO3<NaClO
C.常温下,向Na2S溶液中加入NaCl溶液,S2-的水解程度不受影响
D.向含有Cl-、Br-、I-的混合溶液中滴加AgNO3溶液,先产生黄色沉淀,说明c(I-)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车排放的尾气是大气污染气体之一。如何减少污染气体的排放是科学家研究的热门课题。请回答下列问题:
(1)已知:CO的燃烧热为283.0kJ·mol1,N2(g)+2O2(g) =2NO2(g) ΔH=+64kJ·mol1,则NO2(g)+2CO(g)=![]() N2(g)+2CO2(g) ΔH=___kJ·mol1,若反应中有14g还原剂发生反应,则转移电子___mol。
N2(g)+2CO2(g) ΔH=___kJ·mol1,若反应中有14g还原剂发生反应,则转移电子___mol。
(2)使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
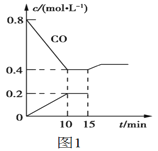
①该反应的化学平衡常数K=___。NO的平衡转化率=___。
②15min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是___。
a.缩小容器体积b.增加CO2的量c.体积不变通入少量氩气d.加入催化剂
③当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是___。
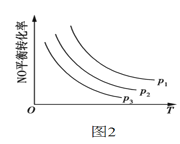
A.该反应ΔH<0 B.p1<p2<p3
C.升高温度正反应速率减小,逆反应速率增大 D.温度不变,增大压强,平衡常数增大
④以下说法中能判断反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)达到平衡的是___。
N2(g)+2CO2(g)达到平衡的是___。
A.反应物和生成物的物质的量相等 B.单位时间内消耗1molNO同时生成1molCO2
C.混合气体压强不再发生变化 D.NO的浓度不再变化
⑤向反应容器中再分别充入下列气体,能使NO转化率增大的是___。
A.O2 B.N2 C.CO D.NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列转化及解释均正确的是( )
转化 | 解释 | |
A | CuS+H2SO4=CuSO4+H2S↑ | 酸性:H2SO4>H2S |
B | AgCl(s)+I-(aq)AgI(s)+Cl-(aq) | Kap(AgCl)<Kap(AgI) |
C | 2Fe+3Cl2 | 氧化性:Cl2>S |
D | C(s,石墨)=C(s,金刚石) △H=+1.9kJ/mol | 稳定性:石墨 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
__C+__K2Cr2O7+__→__CO2↑+__K2SO4+__Cr2(SO4)3+_H2O
请完成并配平上述化学方程式。
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) △H1=-116 kJmol-1
CH3OH(g) △H1=-116 kJmol-1
①下列措施中有利于增大该反应的反应速率的是___;
A.随时将CH3OH与反应混合物分离 B.降低反应温度
C.增大体系压强 D.使用高效催化剂
②已知:CO(g)+![]() O2(g)=CO2(g) △H2=-283 kJmol-1;
O2(g)=CO2(g) △H2=-283 kJmol-1;
H2(g)+![]() O2(g)=H2O(g) △H3=-242 kJmol-1
O2(g)=H2O(g) △H3=-242 kJmol-1
则表示1 mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为___;
③在容积为1 L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系。
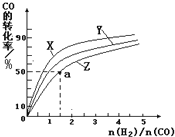
请回答:
ⅰ)在上述三种温度中,曲线Z对应的温度是______;
ⅱ)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=___。
CH3OH(g)的平衡常数K=___。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为7×10-4 mol/L,则生成沉淀所需CaCl2溶液的最小浓度为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com