
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)含500mL 0.8 mol/L 的Al2(SO4)3中所含的SO![]() 的物质的量是___________。
的物质的量是___________。
(2)标准状况下,___________ L NH3所含氢原子数与0.2molH3PO4所含氢原子数相等。
(3)将20ml物质的量浓度为6mol/L的MgSO4加水稀释成100ml溶液,所得稀硫酸的物质的量浓度是_____________。
(4)a个X原子的总质量为bg,则X的相对原子质量可以表示为_______________。
(5)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为__________,质量之比为__________。
(6)等质量的 SO2 和 SO3 物质的量之比是____________,氧原子数之比为____________。
(7)25.4 g某二价金属A的氯化物中含有0.4mol Cl-,则A的摩尔质量为____________。
【答案】1.2 mol 4.48 1.2mol/L ![]() 1:1 4:11 5:4 5:6 56g/mol
1:1 4:11 5:4 5:6 56g/mol
【解析】
根据物质的量公式及阿伏伽德罗定律和推论解答。
(1).含500mL 0.8 mol/L 的Al2(SO4)3中所含的SO![]() 的物质的量=0.5L×0.8mol/L×3=1.2mol,故答案为:1.2mol;
的物质的量=0.5L×0.8mol/L×3=1.2mol,故答案为:1.2mol;
(2).标准状况下,0.2molH3PO4所含氢原子数为0.6mol,要使 NH3所含氢原子数与之相等,则NH3的物质的量为0.2mol,NH3在标准状况下的体积为0.2mol×22.4L/mol=4.48L,故答案为:4.48;
(3).根据稀释时溶质的物质的量不变,即c1v1=c2v2,所以20ml×10-3×6mol/L=c×100ml×10-3,c=1.2mol/L,故答案为:1.2mol/L;
(4).a个X原子的物质的量为:![]() ,则摩尔质量为:
,则摩尔质量为: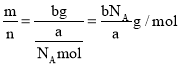 ,故答案为:
,故答案为:![]() ;
;
(5).根据阿伏伽德罗推论有,同温同压,体积之比等于物质的量之比,质量之比等于摩尔质量之比,故答案为:1:1;4:11;
(6).由公式![]() 可知,等质量的 SO2 和 SO3 物质的量之比等于摩尔质量的反比等于5:4,氧原子数之比为5:6,故答案为:5:4;5:6;
可知,等质量的 SO2 和 SO3 物质的量之比等于摩尔质量的反比等于5:4,氧原子数之比为5:6,故答案为:5:4;5:6;
(7).二价金属A的氯化物化学式为ACl2,,含有0.4mol Cl-,则A的物质的量为0.2mol,现A的氯化物质量为25.4g,则A的摩尔质量为56g/mol,故答案为:56g/mol。


科目:高中化学 来源: 题型:
【题目】某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色;J分子内有两个互为对位的取代基.在一定条件下有如下的转化关系:(无机物略去)

(1)属于芳香烃类的A的同分异构体中,其沸点的大小关系为______;(不包括A,用结构简式表示)
(2)J中所含的含氧官能团的名称为______;
(3)E与H反应的化学方程式是________;反应类型是_______;
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的名称是______;
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式_______;
①与FeCl3溶液作用显紫色
②与新制Cu(OH)2悬浊液作用产生红色沉淀
③苯环上的一卤代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝元素在自然界中主要存在于铝土矿(主要成分为A![]() ,还含有F
,还含有F![]() 、FeO、Si
、FeO、Si![]() )中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
)中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
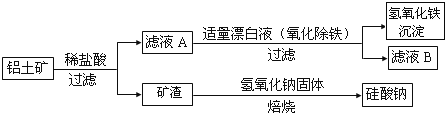
(1)在滤液A中加入漂白液,目的是氧化除铁,便于后期形成Fe(OH![]() 沉淀,所得滤液B显酸性。
沉淀,所得滤液B显酸性。
①检验滤液A中含有F![]() 的试剂为_____
的试剂为_____
②检验滤液B中不含有F![]() 的实验操作方法为_____。
的实验操作方法为_____。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为_____(填选项编号)。
a.氢氧化钠溶液 b.硫酸溶液 c.二氧化碳 d.氨水
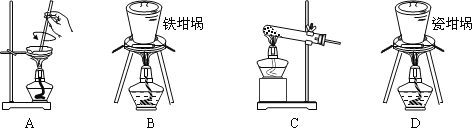
(2)矿渣中一定含有的物质是_____(填化学式)。焙烧制备硅酸钠,可采用的装置为_____(填选项编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ 某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质.
(1)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备。
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙向饱和FeCl3溶液直接加入过量的NaOH溶液。
③丙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
你认为哪位同学的制备方法正确:_______,发生的化学方程式是______________。
(2)Fe(OH)3胶体稳定存在的主要原因是_____。
A.胶粒小,不受重力作用 B.胶粒带同种电荷
C.胶体具有丁达尔效应 D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________________________。
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
Ⅱ 根据如图所示实验装置,回答下列问题:

(1)写出下列仪器的名称:②_________,⑦__________。
(2)上述仪器中实验之前需检查装置是否会漏水的有_________________(填仪器名称)。
(3)利用装置甲制备蒸馏水时,冷凝水应从___________(填“f”或“g”)口进入。
(4)利用装置乙用CCl4从碘水中萃取碘,振荡静置后看到的现象是:________________。
(5)利用装置丁进行实验时,玻璃棒的作用是:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作②的名称是______________,试剂a的溶质是_______________(填化学式)。
(2)加入试剂b所发生反应的化学方程式为_____________________________。
(3)该方案有不足之处,请你把它找出来并改进:_______________________________。
(4)操作③为什么要洗涤沉淀A:_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为____________。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) ===H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(4)Bodensteins研究了下列反应:2HI(g)![]() H2(g) + I2(g)
H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:___________。
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=________min-1
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2/span>)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_________________(填字母)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烃的球棍模型如图所示:

(1)A、B、C的分子式分别是________、________、________;
(2)在120℃、1.01×105Pa时,有两种气态烃和足量的氧气混合点燃,相同条件下测反应前后气体体积,没有发生变化,这两种气态烃是________;
(3)写出B转化为C的化学方程式:_________________________________________________;
(4)除去气体C中混有的少量B可选用的试剂名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z 是同周期主族元素,Y的最外层电子数是X次外层电子数的3倍,四种元素与锂组成的盐是一种新型电池的电解质(结构如图,箭头指向表示共用电子对由W提供,阴离子中所有原子均达到8e-稳定结构)。下列说法不正确的是
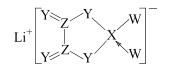
A.该物质中含离子键、极性键和非极性键
B.在四种元素中W的非金属性最强
C.Y和Z两元素形成的化合物不止一种
D.四种元素的原子半径中Z的半径最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)写出实验室制NH3的化学方程式_________________;
(2)写出铅蓄电池的负极电极反应式__________________;
(3)写出Ba(OH)2·8H2O与NH4Cl晶体搅拌反应的化学方程式_______________;
(4)画出稀有气体氪的原子结构示意图__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com