
| A. | ①② | B. | ③④ | C. | ①④ | D. | ②③ |
分析 化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论;
①混合气体的颜色不再改变,说明NO2气体的浓度不变;
②反应前后气体的化学计量数之和不相等,当达到平衡时,气体的压强不变;
③反应速率之比等于化学计量数之比,为正反应速率之比,NO和O2的消耗速率之比为2:1 只能说明反应逆向进行;
④反应达到平衡时的浓度与反应的初始物质的量以及反应的转化程度有关.
解答 解:①混合气体的颜色不再改变,说明NO2气体的浓度不变,达到平衡状态,故①正确;
②反应前后气体的化学计量数之和不相等,当达到平衡时,气体的压强不变,故②正确;
③反应速率之比等于化学计量数之比,故NO和O2的消耗速率之比为2:1不能作为判断是否达到化学平衡状态的依据,故③错误;
④反应达到平衡时的浓度与反应的初始物质的量以及反应的转化程度有关,不能确定是否达到平衡,故④错误;
故选A.
点评 本题考查化学平衡状态的判断,题目难度不大.要注意把握反应特征和平衡状态的理解应用,平衡移动原理是关键.


科目:高中化学 来源: 题型:选择题
| A. | X的氢化物溶于水显酸性且稳定性弱于HF | |
| B. | Y的氧化物是离子化合物,Y的氢氧化物碱性比氢氧化钠弱 | |
| C. | Z的氢化物的水溶液在空气中存放不易变质 | |
| D. | X和Z的最高价氧化物对应的水化物都是弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
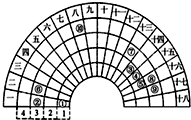 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )| A. | 对应简单离子半径②>⑧>⑨ | |
| B. | 简单氢化物稳定性⑤>⑧ | |
| C. | 最高价氧化物对应的水化物酸性⑨>⑧>⑦ | |
| D. | ①分别与③、④、⑤均可形成既含极性键又含非极性键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌为正极,空气进入负极反应 | B. | 负极反应为:Zn-2e-=Zn2+ | ||
| C. | 正极发生氧化反应 | D. | 正极反应为:Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
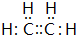 ;
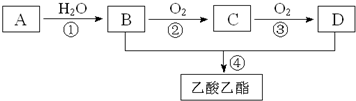
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用不活泼金属铜作电极电解饱和食盐水:2Cl-+2H2O═Cl2↑+H2↑+2OH- | |
| B. | HCO3-离子水解方程式:HCO3-+H2O═H3O++CO32- | |
| C. | 乙烯通入溴水中:C2H4+Br2═CH2BrCH2Br | |
| D. | 氯化铁溶液与碳酸氢钠溶液混合:Fe3++3HCO3-═Fe(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅晶体是一种重要的半导体材料 | |
| B. | 石墨可用做绝缘材料 | |
| C. | 漂白粉的有效成分是次氯酸钙 | |
| D. | 常温下,运输浓硫酸、浓硝酸时可用铝制或铁制槽车 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| C. | 无论怎样控制反应条件,2 mol SO2与1 mol O2 反应时都不会生成2 mol SO3 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 测定某浓度盐酸的pH时,先将pH试纸用蒸馏水湿润 | |
| B. | 容量瓶用蒸馏水洗净、必须烘干后才能用于溶液的配制 | |
| C. | 用苯萃取溴水中的溴之后进行分液时,水层从分液漏斗的下口放出 | |
| D. | 中和滴定时,锥形瓶不需要用待测液润洗后就能使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com