
关于下列各实验装置的叙述中,不正确的是
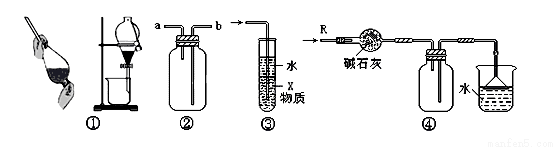
A.装置①可用于分离CH3CHO和H2O的混合物
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上月考二化学卷(解析版) 题型:选择题
36.5gHCl溶液在1L水中(水的密度近似为1g·mL-1),所得溶液的密度为pg·mL-1,质量分数为w,物质的量浓度为c,NA表示阿伏加德罗常数的数值,则下列叙述中正确的是
A.所得溶液的物质的量浓度为c=1mol·L-1
B.所得溶液中含有NA个HCl分子
C.36.5g HCl气体占有的体积为22.4L
D.所得溶液的质量分数:w=36.5c/(1000ρ)
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期第二次月考化学试卷(解析版) 题型:填空题
Ⅰ 能源短缺是人类面临的重大问题。甲醇是一种可再生能源.具有广泛的开发和应用前景。因此甲醇被称为21世纪的新型燃料。
(1)已知在常温常压下:
①2CH3OH(l)十3O2(g) 2CO2(g)+4H2O(g) △H=—1275.6 kJ·mol—1
②H2O(l) H2O(g) △H=+44.0 kJ.mol-1
写出表示甲醇燃烧热的热化学方程式 。
(2)某种甲醇—空气燃料电池是采用铂作为电极,稀硫酸作电解质溶液。其工作时负极的电极反应式可表示为 。
Ⅱ 甲烷也是一种清洁燃料,但不完全燃烧时热效率降低并会产生有毒气体造成污染。
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=―890.3kJ/mol
2CO(g)+O2(g)=2CO2(g) ΔH2=―566.0kJ/mol
(3)则甲烷不完全燃烧生成一氧化碳和液态水时的热效率只是完全燃烧时的________倍(计算结果保留1位小数)。
(4)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol/L的氯化铜溶液的装置示意图:
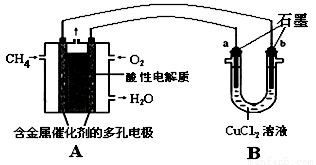
请回答:当线路中有0.1 mol电子通过时,________(填“a”或“b”)极增重________g。
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列情况下,离子组间一定能在溶液中同时大量共存的是
A.pH=2的溶液中:SO42-、K+、NO3-、Mg2+
B.pH试纸呈现红色的溶液:Fe2+、K+、NO3-、Na+
C.水电离出的c(H+)=10-14mol/L的溶液中:Na+、HCO3-、Cl-、SO42-
D.含CO32-可以大量存在的溶液:Ag+、K+、NO3-、Al3+
查看答案和解析>>
科目:高中化学 来源:2016-2017陕西西安长安区一中重点班高一12月考化学卷(解析版) 题型:实验题
某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、KMnO4酸性溶液、MnO2。该同学取一定量Na2O2样品与过量 水反应,待完全反应后,得到溶液X和一定量O2 。
水反应,待完全反应后,得到溶液X和一定量O2 。
(1)写出Na2O2与水反应的化学方程式 。
理论上每消耗7.8g Na2O2转移的电子数为 ,生成的氧气在标况下的体积是 。
(2)该同学推测反应中可能生成了H2O2,并进行实验探究。试设计实验帮助该同学证明溶液X中含过氧化氢 。
(3)通过上述实验证明溶液中确实存在H2O2 ,取少量X于试管中,滴加FeCl 2溶液,立即生成红褐色沉淀,写出反应的离子方程式: ,该反应中H2O2表现了 性(填“氧化”或“还原”)。
2溶液,立即生成红褐色沉淀,写出反应的离子方程式: ,该反应中H2O2表现了 性(填“氧化”或“还原”)。
(4)该同学发现溶液X还可使酸性KMnO4溶液褪色,同时放出氧气,判断该反应中H2O2表现了 性(“氧化”或“还原”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017陕西西安长安区一中重点班高一12月考化学卷(解析版) 题型:选择题
ClO2是一种杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应 制得ClO2:2KClO3 +H2C2O4 + H2SO4=2ClO2↑+ K2SO4 +2CO2↑+2H2O,下列说法正确的是( )
制得ClO2:2KClO3 +H2C2O4 + H2SO4=2ClO2↑+ K2SO4 +2CO2↑+2H2O,下列说法正确的是( )
A.H2C2O4在反应中被还原 B.1mol KClO3参加反应有2mol电子转移
C.ClO2是氧化产物 D.KClO3在反应中得到电子
查看答案和解析>>
科目:高中化学 来源:2016-2017陕西西安长安区一中实验班高一12月考化学卷(解析版) 题型:推断题
下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D 为生活中常见金属单质。(反应过程中生成的水及其他产物已略去)
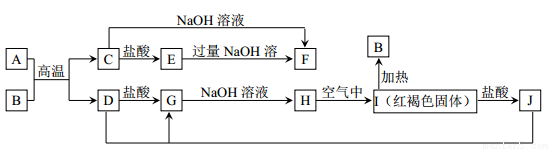
请回答以下问题:
(1)A 是_________,B是_________。(填化学式)
(2)A与B高温反应制得金属 D 的化学反应方程式为________________________。
(3)J的溶液可用来 “刻蚀”铜质电路板,在该刻蚀过程中,所发生反应的离子方程式为_________________________。
(4)检验J中阳离子的试剂是______________________。(写试剂名称)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
某密闭容器中充入一定量SO2、O2,发生反应2SO2+O2 2SO3,测得SO3浓度与反应
2SO3,测得SO3浓度与反应 温度的关系如图所示。下列说法正确的是 ( )
温度的关系如图所示。下列说法正确的是 ( )
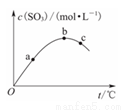
A.该反应ΔH>0 B.SO2转化率:a>b>c
C.化学反应速率:c>b>a D.平衡常数K:b>c>a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com