
| A、5Cl2+I2+6H2O=10HCl+2HIO3 |
| B、2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O |
| C、MnO2+4HCl(浓)=MnCl2+2H2O+Cl2↑ |
| D、2NaCl+2H2O=2NaOH+Cl2↑+H2↑ |
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
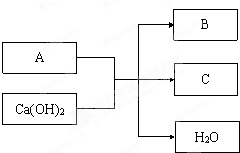
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 物质 | 混有的少量杂质量质质 | 试剂及主要操作 |
| A | 溴苯 | 溴 | 加入苯酚后过滤 |
| B | 硝基苯 | CaCl2 | 蒸馏 |
| C | 乙酸乙酯 | 乙酸 | 加饱和碳酸钠溶液后分液 |
| D | CO2 | CO | 通过灼热的氧化铜 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | Cu→A | +0.15 |
| B | B→Cu | +0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.6g钠与足量水反应,生成Na+离子的数目为0.2NA |
| B、标准状况下,4.48L水中含有H2O分子的数目为0.2NA |
| C、0.3mol 氯气中含有Cl原子的数目为0.3NA |
| D、0.2 mol/L CaCl2溶液中含有Clˉ离子的数目为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com