
科目:高中化学 来源: 题型:
有3份等质量的小苏打,第1份直接与盐酸恰好完全反应;第2份首先加热,使其部分分解后,再与盐酸恰好完全反应;第3份首先加热,使其完全分解后,再与盐酸恰好完全反应。假若盐酸的物质的量浓度相同,消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是( )
A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V1=V2=V3
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:
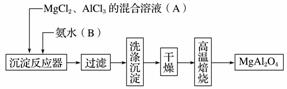
(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入________(填“A”或“B”),再滴加另一反应物。
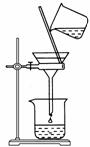
(2)如右图所示,过滤操作中的一处错误是________________。
(3)判断流程中沉淀是否洗净所用的试剂是__________________。高温焙烧时,用于盛放固体的仪器名称是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
结合事实判断CO和N2相对更活泼的是____________,试用下表中的键能数据解释其相对更活泼的原因:____________________。
| CO | C—O | C===O | C≡O |
| 键能(kJ·mol-1) | 357.7 | 798.9 | 1 071.9 |
| N2 | N—N | N===N | N≡N |
| 键能(kJ·mol-1) | 154.8 | 418.4 | 941.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是__________________________________。
(2)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为___________________________________________。
(3)胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:
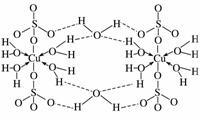
下列有关胆矾的说法正确的是________。
A.所有氧原子都采取sp3杂化
B.氧原子存在配位键和氢键两种化学键
C.Cu2+的价电子排布式为3d84s1
D.胆矾中的水在不同温度下会分步失去
Ⅱ.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1∶3 的个数比配合,还可以其他个数比配合。请按要求填空:
(1)若所得Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显血红色。该离子的离子符号是__________。
(2)若Fe3+与SCN-以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的粒子间的主要相互作用依次是( )
A.氢键;分子间作用力;极性键
B.氢键;氢键;非极性键
C.氢键;极性键;分子间作用力
D.分子间作用力;氢键;非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
(4)H2Se的酸性比H2S________(填“强”或“弱”)。
(5)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:________________;
②H2SeO4比H2SeO3酸性强的原因:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X的基态原子L层电子数是K层电子数的2倍,Y的基态原子最外层电子排布式为nsnnpn+2,则X和Y的气态氢化物中,较稳定的是________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com