
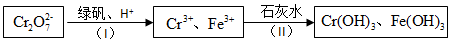
分析 (1)明矾中含有铝离子,易水解生成氢氧化铝胶体,胶体吸附水中的悬浮物而净水;
(2)室温下取0.2mol•L-1HCl溶液与0.2mol•L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,说明得到的盐是强酸弱碱盐;
(3)NaHA溶液中,HA-离子既电离也水解,测得溶液显碱性,说明其电离程度小于水解程度;
(4)依据氧化还原反应离子方程式:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O可以求得Cr2O72-与FeSO4的物质的量之比.
解答 解:(1)明矾溶于水电离出铝离子,铝离子易水解生成氢氧化铝胶体,胶体具有吸附性,能吸附水中的悬浮物而净水,所以明矾能净水,离子方程式为Al3++3H2O?Al(OH)3+3H+,故答案为:Al3++3H2O?Al(OH)3(胶体)+3H+;
(2)等体积等浓度的盐酸和MOH恰好反应生成盐,得到的盐溶液呈酸性,说明该盐是强酸弱碱盐,弱碱电离可逆,其电离方程式为:MOH?M++OH-,
故答案为:MOH?M++OH-;
(3)①NaHA溶液中,HA-离子既电离也水解,电离产生A2-,水解生成H2A,溶液显碱性,说明其电离程度小于水解程度,所以c(H2A)>c(A2-)故答案为:>;
②NaHA溶液中,HA-离子既电离也水解,电离产生A2-,水解生成H2A,溶液显碱性,说明其电离程度小于水解程度,
故答案为:NaHA溶液显碱性,说明其电离程度小于水解程度;
(4)依据氧化还原反应离子方程式:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O可以求得Cr2O72-与FeSO4的物质的量之比为1:6,故答案为:1:6.
点评 本题考查了盐类水解的应用、氧化还原反应计算应用,溶度积的计算应用等知识点,题目难度较大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
| 实验操作 | 预期现象和结论 |
| 取少量反应后固体于试管中,向试管中加入少量水, 将湿润的红色石蕊试纸置于试管口; 另取少量反应后固体于试管中,向试管中加入少量水, 将产生气体通入淀粉-KI溶液中. |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2 L溶液中Ba2+和Cl-的总数为0.8NA | |
| B. | 500 mL溶液中Cl-的浓度为0.2 mol•L-1 | |
| C. | 500 mL溶液中Ba2+的浓度为0.2 mol•L-1 | |
| D. | 500 mL溶液中Cl-的总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 少量的浓硫酸沾到皮肤上时,直接用大量的水冲洗,再涂上稀的NaHCO3溶液 | |
| B. | 为防止试管破裂,加热固体时试管口一般要略低于试管底部 | |
| C. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 | |
| D. | 在盛放浓硫酸的试剂瓶的标签上应印有的警示标记是 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: | B. | HClO的结构式:H-O-Cl | ||
| C. | NF3的比例模型: | D. | H2O2的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+向正极迁移 | |
| B. | 正极反应为:Mo3S4+2xe-═Mo3S${\;}_{4}^{2{x}^{-}}$ | |
| C. | Mo3S4发生氧化反应 | |
| D. | 负极反应为:xMg-2xe-═xMg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
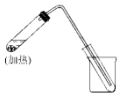 如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
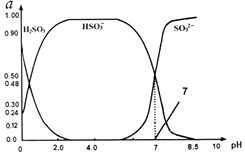 常温下0.1mol•L-1亚硫酸溶液中 H2SO3、HSO3-、SO32-三种微粒所占物质的量分数(a)随pH变化的关系如图所示.下列说法不正确的是( )
常温下0.1mol•L-1亚硫酸溶液中 H2SO3、HSO3-、SO32-三种微粒所占物质的量分数(a)随pH变化的关系如图所示.下列说法不正确的是( )| A. | 由图中数据可计算得到常温下亚硫酸溶液的Ka2 | |
| B. | 在0.1mol•L-1H2SO3溶液中,存在:c2(H+)=c(H+)•c(HSO3-)+2c(H+)•c(SO32-)+Kw | |
| C. | 向pH为7的溶液中滴入少量稀盐酸造成的溶液pH变化小于向pH为4.0的溶液中滴入相同量稀盐酸造成的溶液pH变化 | |
| D. | 在pH=2.0溶液中:c(H2SO3)>c(HSO3-)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com