
分析 原子序数11~17号的元素,为第三周期元素,电子层数相等,随核电荷数的递增,电子层数不变、最外层电子数依次增大、原子半径逐渐减小,元素最高正化合价依次增大,所以随着核电荷数的递增而逐渐变小的是原子半径,以此解答该题.
解答 解:(1)原子序数为11~17号的元素位于第三周期,从左到右,电子层数相同时,随核电荷数增大,原子核对最外层电子的引力增大,则原子半径逐渐减小,
故答案为:减小;电子层数相同时,随核电荷数增大,原子核对最外层电子的引力增大,因此原子半径减小;
(2)原子序数11~17号的元素,为第三周期元素,电子层数相同,原子核外都有3个电子层,故答案为:相同;
(3)同周期元素从左到右,元素的金属性逐渐减弱,非金属性逐渐增强,则得电子能力增强,故答案为:减弱;增强.
点评 本题考查同周期元素性质递变规律、微粒半径比较、原子结构与性质关系等,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意对基础知识的理解掌握.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 用氯气和消石灰制漂白粉 | B. | 铝热法冶炼金属铁 | ||
| C. | 用油脂制肥皂 | D. | 电解水制H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
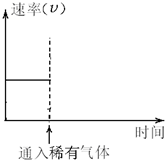 已知一定温度和压强下,在起始容积为V L的容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g)+B(g)?C(g)△H>0.达到平衡时,C的体积分数为40%.试回答:
已知一定温度和压强下,在起始容积为V L的容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g)+B(g)?C(g)△H>0.达到平衡时,C的体积分数为40%.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
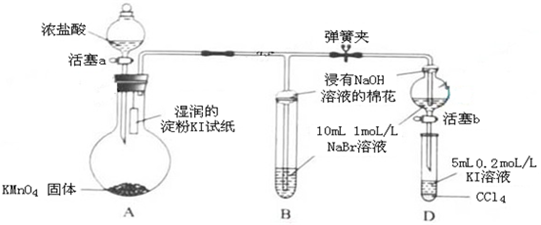
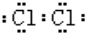 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 向水中加入少量NaOH,平衡逆向移动,c(H+)降低 | |
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol葡萄糖最多可以与5mol金属钠反应放出氢气 | |
| B. | 1mol葡萄糖最多可以与5mol乙酸发生取代反应 | |
| C. | 能发生银镜反应 | |
| D. | 可与小苏打溶液反应冒出气泡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com