
【题目】俄罗斯科学家最近合成第114号元素的原子,该原子的质量数为289,存在时间达到30秒,这项成果具有重要意义.该原子的中子数与质子数之差是( )
A.175
B.114
C.61
D.289
科目:高中化学 来源: 题型:
【题目】短周期元素中:A是地壳中含量最高的元素;B比Ne的质子数多1个;C最外层电子数与其电子层数相等;D单质是半导体材料;E非金属性在同周期元素中最强。下列说法中正确的是
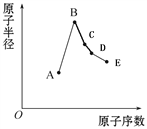
A. B离子的半径比C离子的半径小
B. C单质与A或E单质形成的化合物均为离子化合物
C. A、B两单质反应可得到两种不同的离子化合物
D. B最高价氧化物对应的水化物与0.1mol D单质充分反应放出4.48L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库,含有丰富的化学元素。
(1)在电解饱和食盐水的实验中,阳极产物的检验方法是________________________。
(2)目前从海水中提溴(Br 2 )大致有以下步骤。
①向浓缩的海水中通入Cl2,将海水中的 Br- 氧化为 Br2 。
②用热空气将 Br 2 从上述溶液中吹出,并由浓 Na 2 CO 3 溶液吸收,转变为 NaBr、NaBrO 3和CO2 。吸收1 moL Br 2 需消耗 Na2CO3 ________moL。
③再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式。
____Br— +____ BrO3— +____H + →____ Br2 +____H2O
(3)碘主要从海带中提取,某课外兴趣小组的同学用海带为原料制得少量碘水之后,欲用CCl4从碘水中萃取碘,请简述能用CCl4从碘水中萃取碘的原因是:___________。
(4)同温同浓度的Na2CO3溶液、NaHCO3溶液,PH大小顺序为________ 。NaHCO3溶液中滴入少量氢氧化钠溶液,溶液中c(CO32-)_______(填变大或变小),请用平衡理论解释发生这种变化的原因____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组指定的元素不能形成AB2型化合物的是( )
A. 1s22s22p2和1s22s22p4 B. 1s22s22p63s23p4和1s22s22p4
C. 1s22s22p63s2和1s22s22p5 D. 1s22s22p5和1s22s22p4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件下,对应离子一定能大量共存的是( )
A.在0.1mol/LNaHCO3溶液中:Al3+、NH4+、SO42﹣、NO3﹣
B.常温下, ![]() =0.1mol/L的溶液中:K+ , Cl﹣ , Fe2+ , NO3﹣
=0.1mol/L的溶液中:K+ , Cl﹣ , Fe2+ , NO3﹣
C.使甲基橙变红的溶液中:NH4+ , Cl﹣ , SO2﹣ , Mg2+
D.25℃时,水电离出的c(H+)=1×10﹣13mol/L:K+ , Ba2+ , NO3﹣ , S2﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应中,与其它三个反应的反应类型不同的是
A. CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
B. 2CH3COOH+Mg = (CH3COO)2Mg+H2↑
C. CH4+Cl2 ![]() CH3Cl+HCl
CH3Cl+HCl
D. ![]() +Br2
+Br2![]()
![]() +HBr
+HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示。
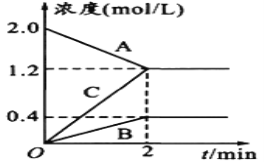
由图中数据
(1)该反应的反应物是___________。
(2)该反应是否可逆反应_____(填“是”或“否”),原因是__________________。写出该反应的化学方程式________________________。
(3)反应开始至2min,用C表示化学平均反应速率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4、CH3OH既是重要的化工原料,又是未来重要的能源物质。
(1)将1.0 mol CH4和2.0 mol H2O(g) 通入容积为2L的反应室,在一定条件下发生反应CH4(g)+H2O(g) ![]() CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
(2)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g) ![]() CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
a.恒容条件下充入He b.增大体积
c.升高温度 d.投入更多的H2O(g)
(3)在恒容条件下进行反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________(填选项序号)。
CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________(填选项序号)。
a.消耗1 mol CO2同时生成1 mol CH3OH b.容器内压强保持不变
c.混合气体的密度保持不变 d.CH3OH(g)的浓度保持不变
(4)以KOH为电解质的甲醇-空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图。 回答下列问题:

①该原电池的正极是____(填“甲”或“乙”),电解过程中乙电极附近pH____(填“增大”或“减小”);
②负极的电极反应式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的项重大贡献。
(1)某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的表现
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性
D.分别做铝片、铜片与NaOH溶液反应的实验
E.将铝片、铜片用导线连接后共同投入稀盐酸中接入电流计,观察电流方向
上述方案中能达到实验目的的是_____________。
(2)现有如下两个反应:A.NaOH+HCl=NaCl+H2O B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是__________(填字母代号),作负极的物质发生了___反应(填“氧化”或“还原”)。
(3)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸一段时间,回答下列问题:

①下列说法正确的是________(填字母代号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___乙(填“>”、“<”或“=”)。原因是______。
③当甲中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com