
| A. | 1mol.L-1的Ca(ClO)2溶液中含ClO-数目为2NA | |
| B. | 22.4LCl2分别与足量的Cu、Fe完全反应转移电子数分别为2NA、3NA | |
| C. | 室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 1 mol-OH与1 molOH-所含电子数均为9 NA |
分析 A、溶液体积不明确;
B、氯气的状态不明确;
C、乙烯和丁烯的最简式均为CH2;
D、羟基不带电荷.
解答 解:A、溶液体积不明确,故溶液中的次氯酸跟的个数无法计算,故A错误;
B、氯气的状态不明确,故氯气的物质的量无法计算,则转移的电子的物质的量无法计算,故B错误;
C、乙烯和丁烯的最简式均为CH2,故21g混合物中含有的CH2的物质的量n=$\frac{m}{M}$=$\frac{21g}{14g/mol}$=1.5mol,则含有的碳原子为1.5NA个,故C正确;
D、羟基不带电荷,故1mol羟基含9mol电子即9NA个;而氢氧根带一个负电荷,故1mol氢氧根含10mol电子即10NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
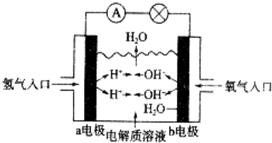
| A. | a电极为负极 | |
| B. | b电极的电极反应式为4OH-→2H2O+O2↑+4e- | |
| C. | 氢氧燃料电池是一种具有应用前景的绿色电源 | |
| D. | 氢氧燃料电池是一种不需要将氧化剂和还原剂全部储藏在电池内的新型发电装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
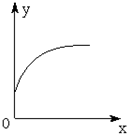 在一密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)?3C(g);△H<0,达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
在一密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)?3C(g);△H<0,达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )| X | Y | |
| A | 增大压强 | C的体积分数 |
| B | 使用催化剂 | C的平衡浓度 |
| C | 充入A | B的转化率 |
| D | 降低温度 | 超过活化能Ea的活化分子百分数 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

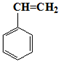
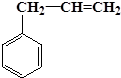
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | ①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝与氧化铁反应既是氧化还原反应,又是吸热反应 | |
| B. | 化学反应中的能量变化只体现为热量的形式 | |
| C. | Ca O+H2O=Ca (OH)2反应过程中,旧键断裂吸收的能量小于新键形成释放的能量 | |
| D. | 外界条件相同时,放热反应的速率一定大于吸热反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
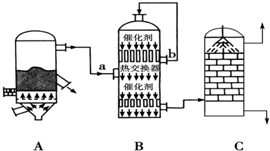
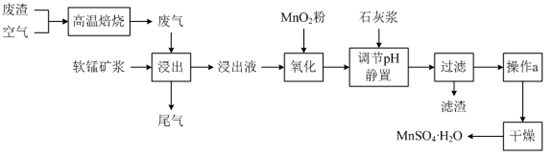
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com