
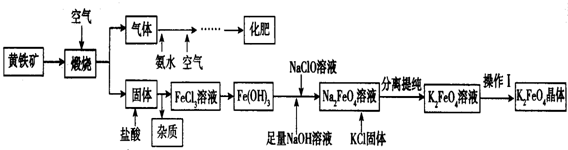
分析 黄铁矿煅烧后生成Fe2O3和SO2,向固体中加入稀盐酸,Fe2O3和HCl反应生成FeCl3和H2O,SiO2不反应,过滤得到滤液,滤液中含有FeCl3,滤渣中含有SiO2,得到的气体通入氨水中并通入空气得到硫酸铵化肥;FeCl3和碱溶液反应得到Fe(OH)3沉淀,在Fe(OH)3中加入足量NaOH溶液、NaClO溶液发生反应生成Na2FeO4,向Na2FeO4溶液中加入KCl固体,发生复分解反应生成K2FeO4,分离提纯得到K2FeO4,通过蒸发浓缩、冷却结晶、过滤得到K2FeO4晶体,
(1)二氧化硫、氨水、氧气发生氧化还原反应生成硫酸铵和水,二氧化硫是还原剂、氧气是氧化剂;
(2)当Fe3+完全沉淀时,c(Fe3+)<10-5mol•L-1,则该溶液中c(OH-)=$\root{3}{\frac{{K}_{sp}[Fe(OH)_{3}]}{c(F{e}^{3+})}}$=$\root{3}{\frac{1.0×1{0}^{-38}}{1{0}^{-5}}}$mol/L=10-11mol/L,溶液中c(H+)=$\frac{1{0}^{-14}}{1{0}^{-11}}$mol/L=0.001mol/L;
Fe(OH)3和NaOH、NaClO发生氧化还原反应生成Na2FeO4、NaCl和水;
(3)高温煅烧黄铁矿时,FeS2和氧气发生氧化还原反应生成氧化铁和二氧化硫;
(4)从溶液中获取晶体采用蒸发浓缩、冷却结晶、过滤的方法;
(5)二氧化硫能使品红溶液褪色,可以用品红溶液检验二氧化硫;
(6)工业上也可用Fe做阳极电解KOH溶液的方法制备K2FeO4,阳极上Fe失电子和OH-反应生成FeO42-和水.
解答 解:黄铁矿煅烧后生成Fe2O3和SO2,向固体中加入稀盐酸,Fe2O3和HCl反应生成FeCl3和H2O,SiO2不反应,过滤得到滤液,滤液中含有FeCl3,滤渣中含有SiO2,得到的气体通入氨水中并通入空气得到硫酸铵化肥;FeCl3和碱溶液反应得到Fe(OH)3沉淀,在Fe(OH)3中加入足量NaOH溶液、NaClO溶液发生反应生成Na2FeO4,向Na2FeO4溶液中加入KCl固体,发生复分解反应生成K2FeO4,分离提纯得到K2FeO4,通过蒸发浓缩、冷却结晶、过滤得到K2FeO4晶体;
(1)二氧化硫、氨水、氧气发生氧化还原反应生成硫酸铵和水,二氧化硫是还原剂、氧气是氧化剂,反应方程式为2SO2+4NH3.H2O+O2=2(NH4)2SO4+2H2O,
故答案为:2SO2+4NH3.H2O+O2=2(NH4)2SO4+2H2O;
(2)当Fe3+完全沉淀时,c(Fe3+)<10-5mol•L-1,则该溶液中c(OH-)=$\root{3}{\frac{{K}_{sp}[Fe(OH)_{3}]}{c(F{e}^{3+})}}$=$\root{3}{\frac{1.0×1{0}^{-38}}{1{0}^{-5}}}$mol/L=10-11mol/L,溶液中c(H+)=$\frac{1{0}^{-14}}{1{0}^{-11}}$mol/L=0.001mol/L,溶液的pH=3;
Fe(OH)3和NaOH、NaClO发生氧化还原反应生成Na2FeO4、NaCl和水,离子方程式为 2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,
故答案为:3; 2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;
(3)高温煅烧黄铁矿时,FeS2和氧气发生氧化还原反应生成氧化铁和二氧化硫,反应方程式为 4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,
故答案为:4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2;
(4)从溶液中获取晶体采用蒸发浓缩、冷却结晶、过滤的方法,所以操作I为蒸发浓缩、冷却结晶、过滤,
故答案为:蒸发浓缩、冷却结晶、过滤;
(5)二氧化硫能使品红溶液褪色,可以用品红溶液检验二氧化硫,其检验方法为将生成的气体通入品红溶液中,褪色,加热,又恢复红色,则气体为二氧化硫,
故答案为:将生成的气体通入品红溶液中,褪色,加热,又恢复红色,则气体为二氧化硫;
(6)工业上也可用Fe做阳极电解KOH溶液的方法制备K2FeO4,阳极上Fe失电子和OH-反应生成FeO42-和水,电极反应式为Fe+8OH--6e-=FeO42-+4H2O,故答案为:Fe+8OH--6e-=FeO42-+4H2O.
点评 本题以化学工艺流程为载体考查物质制备,为高频考点,涉及氧化还原反应、电解原理、物质检验、难溶物溶解平衡、物质分离提纯等知识点,侧重考查学生对化学反应原理、元素化合物知识的理解和掌握及化学知识的综合运用能力,难点是电极反应式的书写,能从整体上把握分析工艺流程是解本题关键,题目难度中等.


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | A | |
| B. | B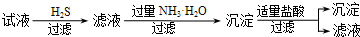 | |
| C. | C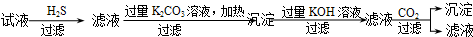 | |
| D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
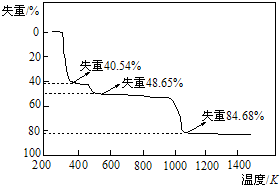
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
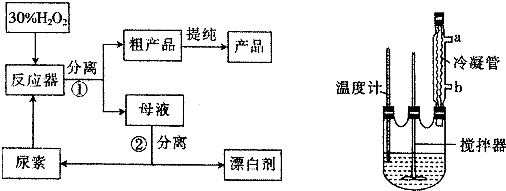
| 分子式 | 外观 | 热分解温度 | 熔点 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75~85℃ |
| 实验序号 | 1 | 2 | 3 | |
| KMnO4溶液的体积/mL | 滴定前读数 | 0.00 | 0.00 | 2.00 |
| 滴定后读数 | 19.98 | 20.00 | 22.02 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
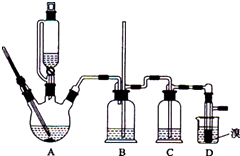 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com