
实验室保存下列试剂的方法不正确的是( )
|
| A. | 钠保存在煤油中 |
|
| B. | 用棕色试剂瓶盛放新制的氯 |
|
| C. | 用带玻璃塞的试剂瓶盛放NaOH溶液 |
|
| D. | 向盛放氯化亚铁溶液的试剂瓶中加少量铁粉 |
| 化学试剂的存放.. | |
| 专题: | 化学实验基本操作. |
| 分析: | A.钠的密度大于煤油且和煤油不反应; B.见光易分解的药品应保存在棕色试剂瓶中; C.烧碱溶液易和二氧化硅反应生成粘性的硅酸钠,液体药品应存放在细口瓶中; D.亚铁离子易被氧化. |
| 解答: | 解:A.金属钠易与空气中氧气反应、易与水反应,与煤油不反应且密度比煤油小,保存在煤油中可隔绝空气,防止钠变质,故A正确; B.因氯水中次氯酸见光容易分解,应用棕色瓶保存,故B正确; C.玻璃中含有SiO2,易与氢氧化钠反应生成具有黏性的硅酸钠而使玻璃塞打不开,保存氢氧化钠溶液时不能用玻璃塞,应用橡皮塞,且溶液应存放在细口瓶中,故C错误; D.硫酸亚铁易被氧化为三价铁离子,可以加入少量的铁粉,防止亚铁离子被氧化,故D正确. 故选C. |
| 点评: | 本题考查化学试剂的保存,明确物质的性质是解答本题的关键,难度不大,注意液体一般保存在细口瓶中,固体保存在广口瓶中. |


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是( )
A.酯化反应是有限度的
B.酯化反应是取代反应的一种
C.酯化反应的产物只有酯
D.浓硫酸可作酯化反应的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
欲配制500 mL 0.2 mol/L的碳酸钠溶液,回答下列问题:
(1)通过计算可知,应用托盘天平称取________g碳酸钠。
(2)称量的操作顺序为________(填选项字母)。
A.调天平零点 B.游码归零 C.向小烧杯中加碳酸钠 D.称量空烧杯 E.向右盘加砝码并将游码移到所需位置 F.将砝码归盒 G.记录称量结果
(3)若砝码和药品位置放颠倒(假设称量时未用烧杯),天平平衡时,实际称量碳酸钠的质量是________。
(4)下列操作使所配溶液浓度偏高的是________。
A.称取28.6 g Na2CO3·10H2O进行配制
B.称量时用了生锈的砝码
C.往容量瓶转移溶液时,有少量液体溅出
D.碳酸钠中含有不溶性杂质
E.未洗涤溶解Na2CO3的烧杯
F.定容时仰视刻度线
G.小烧杯洗净后未干燥即用来称量
H.容量瓶未干燥即用来配制溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 含有离子键和共价键的化合物一定是离子化合物 |
|
| B. | 11H2O.12H2O.13H2O互为同位素 |
|
| C. | 目前人们已发现的元素种类数目与原子种类数目相同 |
|
| D. | 多电子原子中,在离核较近的区域内运动的电子能量较高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
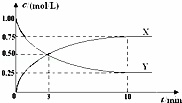
将CO2转化为甲醇的原理为 CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H<0.500℃时,在体积为1L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( )
|
| A. | 曲线X可以表示CH3OH(g) 或H2O(g) 的浓度变化 |
|
| B. | 从反应开始到10min时,H2的反应速率v(H2)=0.225mol/(L﹒min) |
|
| C. | 平衡时H2 的转化率为75% |
|
| D. | 500℃时该反应的平衡常数K=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
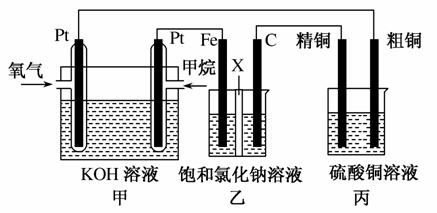
(1)甲烷燃料电池负极反应式是__________________。
(2)石墨(C)极的电极反应式为__________________。
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成的气体体积为________L;丙装置中阴极析出铜的质量为________g。
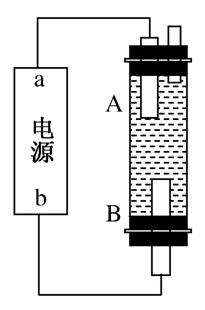
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。
若用于制漂白液,a为电池的________极,电解质溶液最好用________。
若用于制Fe(OH)2,使用硫酸钠作电解质溶液,阳极选用________作电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NaNO2的化学式量为69,则500mL1.0 mol·L-1NaNO2溶液含有溶质质量为
A.13.8g B.69g C. 34.5g D.138g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com