
| A. | 打开啤酒瓶盖,产生大量气泡 | |
| B. | 稀释CH3COOH时,溶液中CH3COO-数目增多 | |
| C. | 工业合成氨常用500℃左右的温度 | |
| D. | 热的纯碱溶液的去污效果比冷的好 |
分析 勒夏特利原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,勒夏特利原理适用的对象应存在可逆过程,如与可逆过程的平衡移动无关,则不能用勒夏特利原理解释.
解答 解:A.打开啤酒瓶盖,压强减小,所以产生大量气泡,能用平衡移动原理解释,故A不选;
B.稀释CH3COOH时,溶液中CH3COO-数目增多,说明加水稀释促进醋酸电离,能用平衡移动原理解释,故B不选;
C.合成氨反应是放热反应,升高温度逆向移动,工业合成氨常用500℃左右的温度,因为此时催化剂催化效果最好,不能用化学平衡移动原理解释的,故C选;
D.盐类水解是吸热反应,升高温度促进盐类水解,所以能用平衡移动原理解释,故D不选;
故选C.
点评 本题考查化学平衡移动原理,为高频考点,明确平衡移动原理适用范围是解本题关键,注意把握影响平衡移动的因素以及使用勒夏特列原理的前提.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有X、Z、W三种含14个电子的粒子,其结构特点如下:
有X、Z、W三种含14个电子的粒子,其结构特点如下:| 粒子代码 | X | Z | W |
| 原子核数目 | 单核 | 同种元素构成的两核 | 同种元素构成的两核 |
| 粒子的电性 | 电中性 | 两个单位负电荷 | 电中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
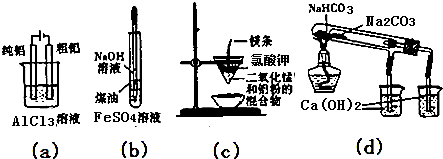
| A. | 用图(a)装置电解精炼铝 | |
| B. | 用图(b)装置制备Fe(OH)2 | |
| C. | 图(c)装置可制得金属钾 | |
| D. | 图(d)验证NaHCO3和Na2CO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
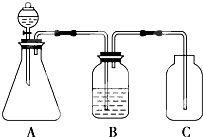
| A. | A中的化学反应可能为:CaCO3+2HCl═CO2↑+CaCl2+H2O | |
| B. | 装置B中盛放的试剂为Na2CO3溶液 | |
| C. | 装置C中盛放的为可溶性硅酸盐 | |
| D. | 由此实验可得到的结构是:酸性HCl>H2CO3>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
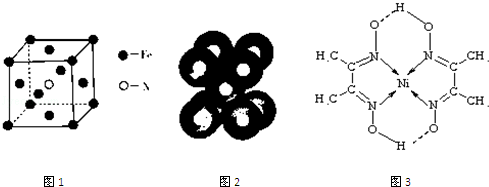
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | B. | c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | ||
| C. | 2c(SO42-)+c(OH-)=c(NH4+)+2c(Fe2+)+c(H+) | D. | c(NH4+)+c(NH3•H2O)=2c(Fe2+)+2c[Fe(OH)2] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
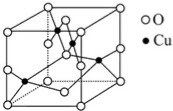 太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等.回答下列问題:
太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等.回答下列问題:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 被提纯的物质 | 选用试剂 | 操作方法 |
| A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
| B | CuSO4(H2SO4) | NaOH溶液 | 过滤 |
| C | CO2(CO) | 氧气 | 点燃 |
| D | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com