
| A. | 5.6L | B. | 11.2L | C. | 16.8L | D. | 22.4L |
分析 根据n=$\frac{m}{M}$计算气体的物质的量,再利用V=n×Vm来计算气体的体积.
解答 解:7gN2的物质的量为n=$\frac{m}{M}$=$\frac{7g}{28g/mol}$=0.25mol,11gCO2的物质的量为n=$\frac{m}{M}$=$\frac{11g}{44g/mol}$=0.25mol,16gSO2的物质的量为n=$\frac{m}{M}$=$\frac{16g}{64g/mol}$=0.25mol,
则气体的总物质的量为0.25mol+0.25mol+0.25mol=0.75mol,标准状况下,该混合气体的体积约为0.75mol×22.4L/mol=16.8L,
故选C.
点评 本题考查气体的体积、物质的量的计算,明确混合气体的总物质的量等于各气体的物质的量之和即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH4+为正四面体形 | B. | CS2为直线形 | ||
| C. | HCN为折线形(V形) | D. | PCl3为三角锥形 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 上述弱酸溶液的 pH=4 | |
| B. | 加入等体积 0.01mol•L-1NaOH 溶液后,所得溶液的 pH=7 | |
| C. | 加入等体积 0.01mol•L-1NaOH 溶液后,所得溶液的 pH>7 | |
| D. | 加入等体积 0.01mol•L-1NaOH 溶液后,所得溶液的 pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
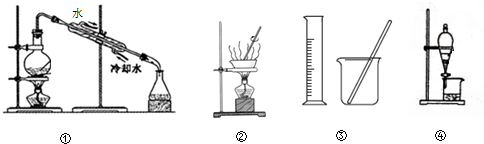
| A. | 用①分离NaCl溶液和NaOH溶液 | |
| B. | 用②蒸干NH4Cl和饱和溶液获取NH4Cl晶体 | |
| C. | 用③配制100mL 0.1000mol•L-1 K2Cr2O2溶液 | |
| D. | 用④分离Na2CO3溶液和CH3COOC2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| C(Fe3+)/mol•L-1 | c(I-)/mol•L-1 | v/mol•L-1•s-1 | |
| ① | 0.80 | 0.20 | 0.032k |
| ② | 0.40 | 0.60 | 0.144k |
| ③ | 0.20 | 0.80 | 0.128k |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
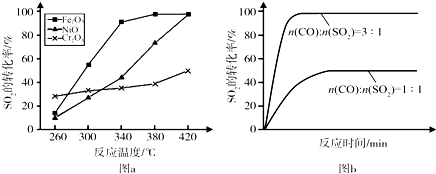
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 步骤 |  |  | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| A. | Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 对此Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com