
����Ŀ����ͼΪ�����������һ�ֺϳ�·�ߣ�

��֪����Ӧ��Ϊȡ����Ӧ����һ��Ӧ����Ϊ�Ҵ�
��ش��������⣺
��1����֪AΪ����������˴Ź��������г���5���䣬�������Ϊ1:1:2:2:2����A������Ϊ___________��
��2��д���йصĻ�ѧ����ʽ
��Ӧ��__________________________��
��Ӧ��__________________________��
��3��������������������ŵ�����Ϊ____________________������������ж���ͬ���칹�壬���б�����ֻ��һ��֧����������NaHCO3��Һ��Ӧ������ʹ������Ȼ�̼��Һ��ɫ��ͬ���칹����__________�֣������������칹����
���𰸡� ����ϩ ![]()
![]() ̼̼˫�������� 8
̼̼˫�������� 8
��������AΪ�����������B�ķ���ʽ��֪��AΪ����ϩ���ұ������ױ���A�ĺ˴Ź��������г���5���壬�������Ϊ1��1��2��2��2����AΪ![]() �����廯�ⷢ���ӳɷ�Ӧ����B��B����±������ˮ�ⷴӦ����C��C������������Ӧ����D��D��������������ͭ����Һ��Ӧ��˵��D�к���ȩ������BΪ
�����廯�ⷢ���ӳɷ�Ӧ����B��B����±������ˮ�ⷴӦ����C��C������������Ӧ����D��D��������������ͭ����Һ��Ӧ��˵��D�к���ȩ������BΪ![]() ��CΪ
��CΪ![]() ��DΪ
��DΪ![]() ��EΪ
��EΪ![]() ����������״�����ȡ����Ӧ����FΪ
����������״�����ȡ����Ӧ����FΪ![]() ��F�������������ȡ����Ӧ����
��F�������������ȡ����Ӧ����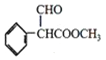 ��
�� �����������ӳɷ�Ӧ����GΪ
�����������ӳɷ�Ӧ����GΪ![]() ��G�ٷ�����ȥ��Ӧ�ð����������
��G�ٷ�����ȥ��Ӧ�ð����������
��1��������������֪��A������Ϊ����ϩ����2����Ӧ�ڵĻ�ѧ����ʽΪ![]() ����Ӧ�۵Ļ�ѧ����ʽΪ��
����Ӧ�۵Ļ�ѧ����ʽΪ��![]() ����3���ɰ���������Ľṹ��֪�������������У�������̼̼˫��������������ж���ͬ���칹�壬���б�����ֻ��һ��֧��������NaHCO3��Һ��Ӧ������-COOH������ʹ������Ȼ�̼��Һ��ɫ������̼̼˫�������Ա���ȡ��ϩ��������Hԭ�ӵõ���ϩ���У�CH2=CHCH2COOH��CH3CH=CHCOOH��CH2=C��CH3��COOH�������ֱ���3��3��2��Hԭ�ӣ��ʷ���������ͬ���칹�干��8�֡�
����3���ɰ���������Ľṹ��֪�������������У�������̼̼˫��������������ж���ͬ���칹�壬���б�����ֻ��һ��֧��������NaHCO3��Һ��Ӧ������-COOH������ʹ������Ȼ�̼��Һ��ɫ������̼̼˫�������Ա���ȡ��ϩ��������Hԭ�ӵõ���ϩ���У�CH2=CHCH2COOH��CH3CH=CHCOOH��CH2=C��CH3��COOH�������ֱ���3��3��2��Hԭ�ӣ��ʷ���������ͬ���칹�干��8�֡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.���������ɡ��ܽ��ת���������Ʊ����ᴿ�Լ����е������й㷺Ӧ�á�
��1����֪25��ʱ��Ksp(BaSO4)��1��10��10����BaSO4������Һ��������Һ��c(Ba2��)��_______mol��L��1��ȡ100 mL��Һ��100 mL 2 mol��L��1��Na2SO4��Һ��ϣ����Һ��c(Ba2��)��___________ mol��L��1��
��2������ʹ�õĹ�¯��Ҫ���ڳ�ˮ��������ή��ȼ�ϵ������ʡ�ˮ���к��е�CaSO4��������Na2CO3��Һ������ʹ֮ת��Ϊ���ɡ����������CaCO3�����������ȥ��
��CaSO4ת��ΪCaCO3�����ӷ���ʽΪ��_____________________________________________________
�������CaSO4ת��ΪCaCO3��ԭ����______________________________________________________
��.��25 ��ʱ��HSCN��HClO��H2CO3�ĵ��볣�����±���
HClO | HSCN | H2CO3 |
K��3.2��10��8 | K��0.13 | K1��4.2��10��7 K2��5.6��10��11 |
��1��1 mol��L��1��KSCN��Һ�У��������ӵ�Ũ���ɴ�С��˳��Ϊ_________________________________
��2����Na2CO3��Һ�м������HClO��Һ����Ӧ�Ļ�ѧ����ʽΪ_______________________________
��3��25 ��ʱ��Ϊ֤��HClOΪ���ᣬijѧϰС���ͬѧ�������������ʵ�鷽�����������ַ����У�����Ϊ�ܹ��ﵽʵ��Ŀ�ĵ���______________________(�����и��������)��
a����pH�Ʋ���0.1mol��L��1NaClO��Һ��pH�������pH>7����֤��HClOΪ����
b����pH��ֽ����0.01 mol��L��1 HClO��Һ��pH�������pH>2����֤��HClOΪ����
c������������Ũ�Ⱦ�Ϊ0.1 mol��L��1��HClO��Һ������ĵ����ԣ������HClO��Һ�ĵ������������ᣬ��֤��HClOΪ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д��ȷ���ǣ�������
A. �ƺ���ˮ��ӦNa+2H2O��Na++2OH-+H2��
B. ��������������������ҺAl+2OH-��AlO2-+H2��
C. ����������������2Al+6H+��2Al3++3H2��
D. ����ϡ���ᷴӦ2Fe+6H+��2Fe3++3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�������ֺ��أ�1H��2H��3H����Ԫ�������ֺ��أ�35Cl��37Cl����������ɵ��Ȼ�����ӵ�������
A. 5�� B. 6�� C. 7�� D. 8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵĹ�ҵ��ˮ�Ĵ���������ͼ��ʾ��

(1)������ͼ�豸���н��е���________����(��д��������)��ʵ��������һ������������________(����������)���С�
�����豸���з�����Ӧ�Ļ�ѧ����ʽΪ________________________��
(2)Ϊ�˷�ֹˮԴ��Ⱦ���ü����������Եķ�������ij�����ŷŵ���ˮ�����ޱ��ӣ��˷�����_______________________________________��
(3)Ϊ�ⶨ��ˮ�б��ӵĺ�����ȡ�˷�ˮ100 mL�������м���Ũ��ˮ�����ٲ�������Ϊֹ���õ�����0.331 g���˷�ˮ�б��ӵĺ���Ϊ______mg��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֻ��һ���Լ����ܼ����AgNO3��Na2SO4��Na2CO3������Һ��Ӧѡ��
A. BaCl2 B. HCl C. NaOH D. NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵһ����˵��HF���������
����������NaF��Һ��pH����7��������HF��Һ��������ʵ�飬���ݺܰ���
����HF��NaCl���ܷ�����Ӧ��������������0.1mol/L��HF��Һ��pHΪ2.3��
��HF����Na2CO3��Һ��Ӧ������CO2���壻��HF��ˮ��������Ȼ��ܣ�
��1mol/L��HFˮ��Һ��ʹ��ɫʯ����Һ��졣
A. �٢ڢ� B. �ڢۢ� C. �ۢܢ� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йط�Ӧ�ȵ���������ȷ����
�ټ�֪2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ/mol����������ȼ����Ϊ��H��-241.8kJ/mol
���ɵ���Aת��Ϊ����B��һ�����ȹ��̣��ɴ˿�֪����B�ȵ���A�ȶ�
��X(g)��Y(g) ![]() Z(g)��W(s) ��H>0�����º��������´ﵽƽ������X��������Ӧ�ġ�H����
Z(g)��W(s) ��H>0�����º��������´ﵽƽ������X��������Ӧ�ġ�H����
�ܼ�֪��![]()
�ϱ����ݿ��Լ����![]() ���ʱ�
���ʱ�
�� ���ݸ�˹���ɣ���֪����ͬ�����£����ʯ��ʯīȼ������1molCO2����ʱ���ų����������
A. �٢ڢ� B. �ܢ� C. �� D. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�о��������ϳɰ���Ӧ��T��ʱ�����ݻ�Ϊ2 L����������ͨ��4 mol N2��12mol H2����Ӧ���£� N2(g)+3H2(g) ![]() 2NH3(g) ��H=-92.0kJmol-1����ؼ����������£�
2NH3(g) ��H=-92.0kJmol-1����ؼ����������£�
N��N | H-H | N-H | |
��������( kJ/mol) | 946 | 436 | X |
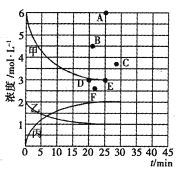
��25minʱ��Ӧ�ﵽƽ�⣬������Ũ����ʱ��仯��������ͼ�мס��ҡ������ش��������⣺
(1)0-25min�ڣ���Ӧ��ƽ������v(H2)Ϊ_________������X=_________________��
(2)T��ʱ���÷�Ӧ��ƽ�ⳣ��K=_____________ ���������������
(3)T��ʱ������ʼ����8mol N2��24 mol H2����Ӧ�մﵽƽ��ʱ����ʾc( H2)����ͼ����Ӧ�ĵ�Ϊ_____������ĸ����
(4)��úΪ��Ҫԭ�ϵĺϳɰ���ҵ�У�ԭ����������������������ã�
��C(s) +H2O(g)![]() CO(g) +H2(g) ��H1
CO(g) +H2(g) ��H1
��CO(g) +H2O(g)![]() CO2(g) +H2(g) ��H2
CO2(g) +H2(g) ��H2
����֪CO��H2��ȼ���ȷֱ�Ϊ283 kJ��mol-l��285.8kJ��mol-l��H2O( g) =H2O(1) ��H =-44kJ��mol-l ���H2=_______________��
(5)�����������������Ҫԭ�ϣ���������£�
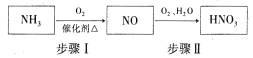
д������I�Ļ�ѧ����ʽ��_________________��
(6)��ͼ�ǿ�ѧ����������õ�ⷨ���³�ѹ���ɵ����������ϳɰ���ʾ��ͼ��
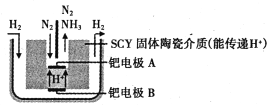
��ͼ��֪���ٵ缫B�ǵ��ص�________����������������������ٵ缫A�ϵĵ缫��ӦʽΪ________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com