
| A. | 燃烧产物只有CO2和H2O | B. | 与卤素单质发生取代反应 | ||
| C. | 都溶于水 | D. | 通常不与强酸、强碱、强氧化剂反应 |
科目:高中化学 来源: 题型:解答题
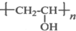 ,其工业合成路线如下:
,其工业合成路线如下: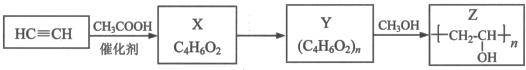
 ;
;
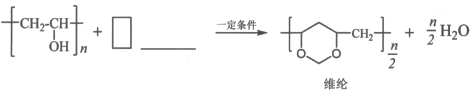
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
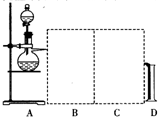
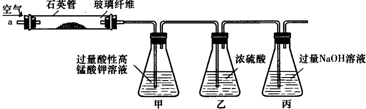
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 这两种烃一定是同分异构体 | |
| B. | 这两种烃不可能是同系物 | |
| C. | 在这两种烃的分子中,碳、氢原子个数之比一定相同 | |
| D. | 这两种烃各1mol完全燃烧,生成水的质量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 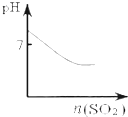 可表示将SO2气体通入氯水时pH的变化 | |
| B. |  表示KNO3的溶解度曲线,a点是80℃的KNO3的不饱和溶液 | |
| C. | 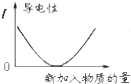 表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 | |
| D. | 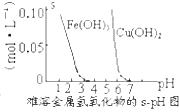 根据图,除去CuSO4溶液中Fe3+,可加氨水调节pH=4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | E、C、D、B、A | B. | D、B、C、A、E | C. | E、B、A、D、C | D. | A、B、C、D、E |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浊液中存在沉淀溶解平衡:AgCl(s)?Ag+(aq)+CI-(aq) | |
| B. | 实验可以证明NH3结合Ag+能力比Cl-强 | |
| C. | 实验表明实验室可用氨水洗涤银镜反应后的试管 | |
| D. | 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com