
| A. | 三种元素的原子序数 Y>X>Z | |
| B. | 三种元素的原子半径 X>Y>Z | |
| C. | 同周期元素中X的金属性最强 | |
| D. | 同周期元素中Z的最高价氧化物的水化物酸性最强 |
分析 X+与Z2-具有相同的核外电子层结构,X+与Z2-具有相同的核外电子层结构,则X为第ⅠA族元素,Z为第ⅥA族元素,且X在Z元素的下一周期,由于为短周期元素,故X处于第三周期、Z处于第二周期,则X为Na、Z为O;又因为X、Y、Z原子序数之和为35,则Y的原子序数=35-8-11=16,故Y为S,结合元素周期律的递变规律解答该题.
解答 解:X+与Z2-具有相同的核外电子层结构,X+与Z2-具有相同的核外电子层结构,则X为第ⅠA族元素,Z为第ⅥA族元素,且X在Z元素的下一周期,由于为短周期元素,故X处于第三周期、Z处于第二周期,则X为Na、Z为O;又因为X、Y、Z原子序数之和为35,则Y的原子序数=35-8-11=16,故Y为S.
A.X为Na、Z为O、Y为S,原子序数Y>X>Z,故A正确;
B.同周期自左而右原子半径减小,同主族自上而下原子半径越大,故原子半径Na>S>O,故B正确;
C.同周期自左而右金属性减弱,故第三周期中Na的金属性最强,故C正确;
D.Z为氧元素,不存在含氧酸,故D错误,
故选D.
点评 本题考查原子结构与元素周期律,推断元素是解题关键,侧重对元素周期律的考查,D选项为易错点,注意O、F元素没有含氧酸.


科目:高中化学 来源: 题型:选择题
| A. | 用红外光谱法鉴别乙醇和二甲醚 | |
| B. | 用酸性高锰酸钾溶液鉴别乙烷和乙炔 | |
| C. | 用溴水鉴别苯和四氯化碳 | |
| D. | 用溴水鉴别苯和甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3与石灰水反应当n(NaHCO3):n[Ca(OH)2]=1:1时HCO3-完全转化为CaCO3 | |
| B. | CO2通入石灰水中,当n(CO2):n[Ca(OH)2]=1:1时,能得到澄清溶液 | |
| C. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=1:1时铝元素以AlO2-形式存在 | |
| D. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,溶液中存在Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2Se(硒化氢)比H2S稳定 | B. | Si、Ge(锗)均可做半导体材料 | ||
| C. | Mg(OH)2的碱性比Be(OH)2的弱 | D. | H3BO3(硼酸)的酸性比H2CO3的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 电能是现代社会应用最广泛的能源之一.原电池是一种将化学能转化为电能的装置.如图所示的锌、铜和稀硫酸组成的原电池中,锌片上发生氧化反应(填“氧化”或“还原”).铜片上的电极反应式是2H++2e-=H2↑.能否根据反应NaOH+HCl=NaCl+H2O 设计成原电池,否(填“能”或“否”),原因是该反应不是氧化还原反应,没有电子转移.
电能是现代社会应用最广泛的能源之一.原电池是一种将化学能转化为电能的装置.如图所示的锌、铜和稀硫酸组成的原电池中,锌片上发生氧化反应(填“氧化”或“还原”).铜片上的电极反应式是2H++2e-=H2↑.能否根据反应NaOH+HCl=NaCl+H2O 设计成原电池,否(填“能”或“否”),原因是该反应不是氧化还原反应,没有电子转移.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2与水反应 | |
| B. | 氨气与水反应 | |
| C. | 工业合成氨 | |
| D. | 水电解生成H2和O2与H2在O2中燃烧生成H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
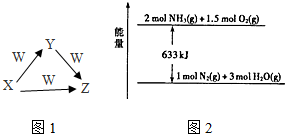 X、Y、Z、W为中学化学常见的物质,它们之间的转化关系如图所示.请填写下列空白.
X、Y、Z、W为中学化学常见的物质,它们之间的转化关系如图所示.请填写下列空白. 3CO2+2Fe.(用化学方程式表示)
3CO2+2Fe.(用化学方程式表示)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com