
| A. | 在游泳池中常加CuSO4和漂白粉,它们使细菌蛋白质变性的原理相同 | |
| B. | 铜制品在潮湿空气中生锈,其主要原因是发生吸氧腐蚀 | |
| C. | “地沟油”禁止食用,但可以用来制肥皂,是利用了皂化反应 | |
| D. | 利用K2FeO4作水处理剂是因为它既有吸附性又有强氧化性 |
分析 A.铜离子为重金属离子,漂白粉有强的氧化性,据此解答;
B.潮湿空气中,铜与杂质容易形成原电池;
C.油脂碱性条件下水解,可生成肥皂;
D.K2FeO4具有强的氧化性,还原生成的三价铁离子水解生成具有吸附性的氢氧化铁胶体,据此解答.
解答 解:A.在游泳池中常加CuSO4和漂白粉,它们使细菌蛋白质变性的原理不相同,铜离子因为其为重金属离子,漂白粉中次氯酸钙具有强的氧化性,故A错误;
B.潮湿空气中,铜与杂质容易形成原电池,发生吸氧腐蚀,故B正确;
C.地沟油的主要成分是油脂,油脂碱性条件下水解成为肥皂,该反应为皂化反应,可生成肥皂,故C正确;
D.高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,故D错误;
故选:BC.
点评 本题考查了元素化合物知识,明确蛋白质变性方法、优质的性质、原电池工作原理是解题关键,题目难度不大.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源: 题型:解答题
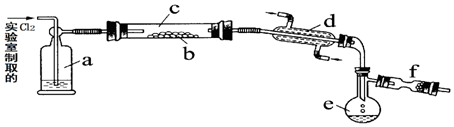
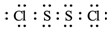 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
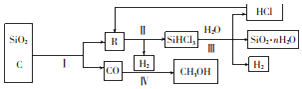
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原料来源广 | B. | 易燃烧,放出热量多 | ||
| C. | 产物无污染 | D. | 制取H2简单易行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
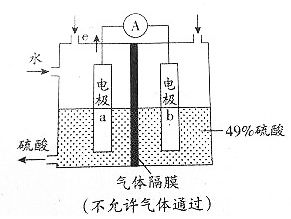
| A. | 该装置工作时能将化学能转化为电能,并有H2SO4生成 | |
| B. | 电极b表面O2发生还原反应,电极b附近溶液的pH升高 | |
| C. | 气体样品从电极a区域通入,样品中的SO2在电极a表面得到电子 | |
| D. | 电极a表面发生的电极反应时为SO2+2H2O-2e-=${SO}_{4}^{2-}$+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6g | B. | 11.2g | C. | 16.8g | D. | 22.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
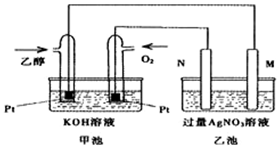 已知甲醇、乙醇都是重要的有机化工原料,回答下列问题:
已知甲醇、乙醇都是重要的有机化工原料,回答下列问题:| 化学反应及平衡常数 | 平衡常数数值 | ||
| 500℃ | 800℃ | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | 2.5 | 0.375 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com