
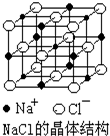
 NaCl晶体结构如图所示,现测知NaCl晶体中Na+与Cl-平均距离为a cm,该晶体密度为ρg•cm-3,则阿伏加德罗常数可表示为( )
NaCl晶体结构如图所示,现测知NaCl晶体中Na+与Cl-平均距离为a cm,该晶体密度为ρg•cm-3,则阿伏加德罗常数可表示为( )| A. | $\frac{0.585}{4{a}^{3}ρ}$ | B. | $\frac{5.85}{8{a}^{3}ρ}$ | C. | $\frac{58.5}{2{a}^{3}ρ}$ | D. | $\frac{58.5}{{a}^{3}ρ}$ |
分析 NaCl晶体中Na+与Cl-平均距离为a cm,则晶胞棱长为2a cm,晶胞中Na+离子数目为1+12×$\frac{1}{4}$=4、Cl-离子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则晶胞质量为4×$\frac{58.5g/mol}{{N}_{A}mo{l}^{-1}}$,再结合m=ρV计算.
解答 解:NaCl晶体中Na+与Cl-平均距离为a cm,则晶胞棱长为2a cm,晶胞体积为(2a cm)3,晶胞中Na+离子数目为1+12×$\frac{1}{4}$=4、Cl-离子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则晶胞质量为4×$\frac{58.5g/mol}{{N}_{A}mo{l}^{-1}}$,则ρg•cm-3×(2a cm)3=4×$\frac{58.5g/mol}{{N}_{A}mo{l}^{-1}}$,解得NA=$\frac{58.5}{2{a}^{3}ρ}$,
故选:C.
点评 本题考查晶胞计算,关键是计算晶胞质量,理解掌握均摊法进行晶胞有关计算,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
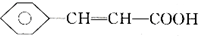 ),继而合成H的路线如下:
),继而合成H的路线如下: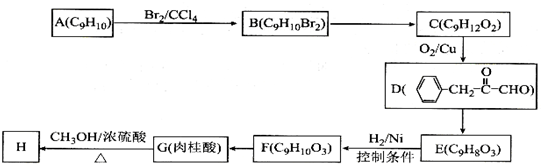
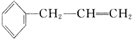 ,D中含有官能团的名称为羰基、醛基;
,D中含有官能团的名称为羰基、醛基; +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$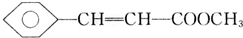 +H2O;
+H2O;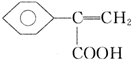 、
、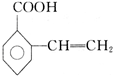 、
、 、
、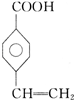 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
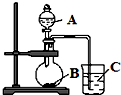 某研究性学习小组设计了一组实验,验证元素周期律.
某研究性学习小组设计了一组实验,验证元素周期律.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向偏铝酸钠溶液中加入过量盐酸:AlO2-+4H+=Al3++2H2O | |
| B. | MnO2与浓盐酸混合加热:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| C. | 等浓度等体积的Ba(OH)2溶液和NaHSO4溶液混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| D. | 用NaOH溶液吸收少量H2S气体:OH-+H2S=HS-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
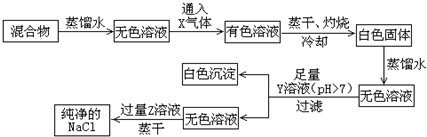
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锡中加入一定量的铅制成焊锡,目的使被焊接的部分更牢固,更不易被氧化 | |
| B. | 聚乙烯制成塑料薄膜,用于食品、药品包装的材料 | |
| C. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,下层液体从分液漏斗下口放出,上层液体从上口倒出 | |
| B. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| C. | 蒸馏操作时,使用的冷凝水应该由低往高流,形成逆流 | |
| D. | 蒸发操作时,应使混合物中的水分子蒸干后,才能停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com